где: R1 и R2 является низшей алкильной группой, R3, R - низшая алкоксигруппа, кольцо А - замещенное бензольное кольцо формулы:
ИЛИ R90
ИЛИ
R6, R7, R8, R9. R10- низшая алкильная группа, или его фармацевтически приемлемой соли, заключающийся во взаимодействии низшего алкилацетилендикарбоксилата формулы:
ОО
1 II ROCI о C5C-C-OR (II)
где: R и R2 - указаны выше, с производным бензальдегида или его динизшего алкила- цеталя формулы:
OR5 (Щ)
OR5 - низшая алкокси- или алканоилоксиг- руппа, кольцо A, R , R -определены выше, при нагревании до температуры 60-80°С в присутствии кислоты, в качестве которой используют низшую тригалоидалкановую кислоту процесс проводят с использованием 1-2 эквимолярного количества карбоксила- та по отношению к бензальдегиду, после чего полученный продукт при необходимости переводят в соль,
Отличительными признаками процесса является то, что в качестве производного бензальдегида используют производное общей формулы
OR - низшая алкокси или алканоилоксиг- руппа, кольцо A, R3, R - определены выше, в качестве кислоты - низшую тригалоидалкановую кислоту и проведение процесса с использованием 1-2 эквимолярного количества карбоксилата по отношению к бензальдегиду, что позволяет упростить процесс и повысить его селективность.
5
0
5
0
5
0
5
0
5
В качестве низшей тригалоидной кислоты используют трифторуксусную кислоту.
Окси-группу защищают с помощью низшей элкильной или низшей алканоильной группы.
Соединение I может быть, если это необходимо, затем превращено в соль щелочного металла, соль щелочно-земельного металла или четвертичную соль аммония при помощи известных приемов.
Предлагаемый процесс позволяет использовать в качестве исходного соединения - производное бензальдегида (II), которое содержит защищенную окси-группу в «-позиции бензиловой составляющей, что отличает его от способа-прототипа.
Предлагаемый способ имеет то преиму- щество, что соединение I может быть получено с высоким выходом без побочных продуктов и, кроме того, что использование исходного соединения (II) или его низшего диалкилацеталя не сопровождается существенной полимеризацией из-за присутствия свободной оксигруппы в течение реакции и/или при его хранении.
Кроме того, исходное соединение (III), в котором OR является низшей алканоилок- си-группой, может быть легко получено в форме кристаллов при помощи простой рекристаллизации из стандартного растворителя (например, изопропилового простого эфира) и эффективно использовано для реакции с соединением ацетилендикар- боксилэта (II); в то время как низший диал- килацеталь незащищенного соединения а-оксибензилбензапьдегида в общем случае получают в виде масла, которое трудно очистить.
Альдегид (III) и его низший диалкилаце- таль, используемый в качестве исходного соединения в соответствии с настоящим изобретением, могут быть легко получены в результате взаимодействия соответствующего соединения а-оксибензилбензальде- гида или его низшего диалкилацеталя с низшим алкилгалоидом, химически активным производным низшей алкановой кислоты (например, активными сложными эфирами, галидами и ангидридами кислот низшей алкановой кислоты) и т.д. в присутствии акцептора кислоты.
Пример1.5,Ог2-( «-окси-3,4-диметок- сибензил)-3,4,5-триметоксибензальдегид диметилацеталя растворяют в 50 мл меги- ленхлорида. В раствор добавляют 3,8 мл триэтиламина, 3,0 мл уксусного ангидрида и 100мг 4-диметиламинопиридина. Смесь перемешивают при комнатной температуре я течение 3 дней. Реакционную смесь промывзют, сушат и выпаривают, чтобы удалить растворитель, при этом получают .5,2 г 2-(а- ацетокси-3,4-диметоксибензил)-3,4,5-три- метоксибензальдегид диметилацетэля
(Ш).
ЯМР(, (5): 2.17 (синглет, ЗН), 3,11 (синглет, ЗН),.3,47 (синглет, ЗН), 3,74 (синглет, ЗН), 3,79 (синглет, ЗН), 3,83 (синглет, ЗН), 3,86 (синглет, ЗН), 3,88 (синглет, ЗН), 5,53 (синглет, 1Н), 6,55-6,95 (мультиплет, ЗН), 7,00 (синглет, 1 Н), 7,38 (синглет, 1Н).
5,2 г диметилацеталя растворяют в смеси 100 мл тетрагидрофурэна и 20 мл воды. В раствор при охлаждении льдом добавляют 9 мл 10% хлористоводородной кислоты и смесь перемешивают при той же температуре в течение 2 часов. В реакционную смесь добавляют охлажденную воду и смесь экстрагируют этилацетатом. Экстракт промывают, сушат и выпаривают, чтобы удалить растворитель. Полученный в результате остаток подвергают очистке при помощи хроматографической колонны на силикагеле (растворитель: толуол-этил ацетат (5; 1)) и подвергают рекристаллизации из изопропилового простого эфира, при этом получают 4,27 г 2-{ а-ацетокси-3,4-диметок- си-бензил 3,4,5-триметоксибензальдегида в виде бесцветных кристаллов (III).
Температура точки плавления: 96-98°С. Нуйол. ИК макс, (): 1740, 1680.
780 мг продукта (III) растворяют в 20 мл бензола. В раствор добавляют 0,7 мл диме- тилацетилендикарбоксилата (II) и 5 мл трифторуксусной кислоты. Смесь перемешивают при температуре 60°С в течение 4 часов и выпаривают, чтобы удалить растворитель. В полученный в результате остаток добавляют метанол и кристаллический осадок отфильтровывают, при этом получают 750 мл 1-{3,4-диметоксифенил}-2,5-бис- (метоксикарбонил)-4-окси-6,7,8-триметокси нафталина (I) в виде бесцветных призм. Выход: 77%. Температура точки плавления: 178-179°С.
2-(ес-ацетокси-3,4-диметоксибенз 1л)3, 4,5-триметоксибензальдегид подвергают взаимодействию с диметилацетилендикар- боксилатом по той же схеме.
Получают 1(3,4-диметоксибензил)-3,4,5- триметоксибензальдегид, подвергают взаимодействию с диметияацетилацетиленди- карбоксилатом по той же схеме.
Получают 1-(3,4-диметоксифенил)-2,3- бис(метоксикэрбонэл}-4-окси-6.7,8-триме,- токсинафтаяин (I).
Полученный таким образом продукт имеет те же физико-химические свойства,
Раствор 4,86 г продукта (I) в 100 мл тет- рагидрофурана добавляют в раствор 0,387 г 62,5% раствора гидрида натрия в 10 мл тет1 рагидрофурана при комнатной температуре 5 при перемешивании. Смесь перемешивают при той же температуре в течение одного часа и выпаривают при пониженном давлении при температуре ниже 30°С. Полученный в результате остаток растирают с
0 петролейным эфиром, при этом 4,8 г соли натрия 1-{3,4-диметоксифенил)-2,3-бис(ме- токсикарбонил)-4-ркси-6,7,8-триметоксина- фталина получали в виде порошка. ИК VMBKC. (см-1): 1710, 1680, 1600.
5 П р и м е р 2. 0,93 г 2-{а-окси-3,4-диме- токсибензил)-3,4.5-триметоксибензэльде- гиддиметил.ацеталя растворяют в 15 мл тет- рагидрофурана. В раствор по каплям добавляют суспензию 65 мг гидрида натрия
0 в 10 мл диметилформамида и смесь перемешивают при комнатной температуре в течение 3 ч. После того, как реакцию охлаждали льдом, в нее добавляли 0,17 мл метил иодида. Смесь перемешивают при комнатной тем5 пературе в течение 16 часов и выпаривают, чтобы удалить растворитель. Полученный в результате остаток сливают в смесь водного насыщенного раствора бикарбоната натрия и диэтилового простого эфира, .при этом
0 получают органический слой. Водный слой затем экстрагируют диэтиловым простым эфиром, а экстракт соединяют с органическим слоем, промывают, сушат и выпаривают, чтобы удалить растворитель, при этом
5 получают 0,87 г 2-( а-метокси-3,4,-диметок- сибензил)-3,4,5-триметокеибензальдегид диметилацеталя.
ЯМР (СОС)з, д ): 2,91 (синглет, ЗН), 3.40 (синглет, 6Н), 3,77 (синглет, ЗН), 3,84 (синг0 лет, 6Н). 3,89 (синглет, 6Н), 5,43 (синглет, 1Н), 5,90 (синглет. Ж), 6,65-7.05 (мультиплет, ЗН).
0,87 г полученного продукта растворяют в 30 мл тетрагидрофурана. В раствор добав5 ляют 20 мл 0,001 М хлористоводородной кислоты и смесь перемешивают при комнатной температуре в течение 80 мин. Реакционную смесь выпаривают, чтобы удалить растворитель, а полученный в результате
0 остаток встряхивают со смесью этилацетата и воды. Получают органический слой, который промывают, сушат и выпаривают растворитель. Остаток подвергают обработке на хроматографической колонне на сили5 кагеле (растворитель:толуол:этилацетат (10:1)) и элюат выпаривают, чтобы удалить растворитель, при этом получают 680 мг 2-( а -метокси-3,4-диметоксибензил)-3.4,5-три- метоксибензальдегида (III).
ЯМР (СОС1з, д): 3,39 (синглет, ЗН), 3,82 (синглет, ЗН), 3,83 (синглет, ЗН). 3,86 (сииг- лет, ЗН), 3,91 (синглет, ЗН), 3,9.7 (синглет, ЗН). 5.99 (синглет, 1Н), 6,55-7,05 (мульти- плет, ЗН), 7,37 (еинглет, 1Н), 10.32 (синглет. 1Н)..
220 мг продукта (III) растворяют в 10 мл бензола. В раствор добавляют 0,11 млдиме- тилацетилендикарбоксилата и 0,002 мл трифторуксусной кислоты, и смесь подвергают дефлегмации в течение 30 мин. Реакционную смесь выпаривают, чтобы удалить растворитель, а в полученный в результате остаток добавляют метанол. Кристаллический осадок собирают фильтрацией, при этом получают 160 мг 1-{3,4-диметоксифе- нил)-2,3-бис(метоксикарбонил)-4-оксй-6,7, 8-триметоксинафталина в виде бесцветных призм.
Фильтрат подвергают очистке с использованием хроматографической колонны на силикагеле (растворитель: этилацетат:толу- ол), а элюат выпаривают, чтобы удалить растворитель, в результате чего получают 40 мг 1-(3,4-диметоксифенил}-2,3-бис(метоксикар- бонил)-4-окси-6,7,8-триметоксинафталина (дополнительно).
Выход: 70%.
Полученный таким образом продукт имел такие же физико-химические свойства, что и продукт из примера 1.
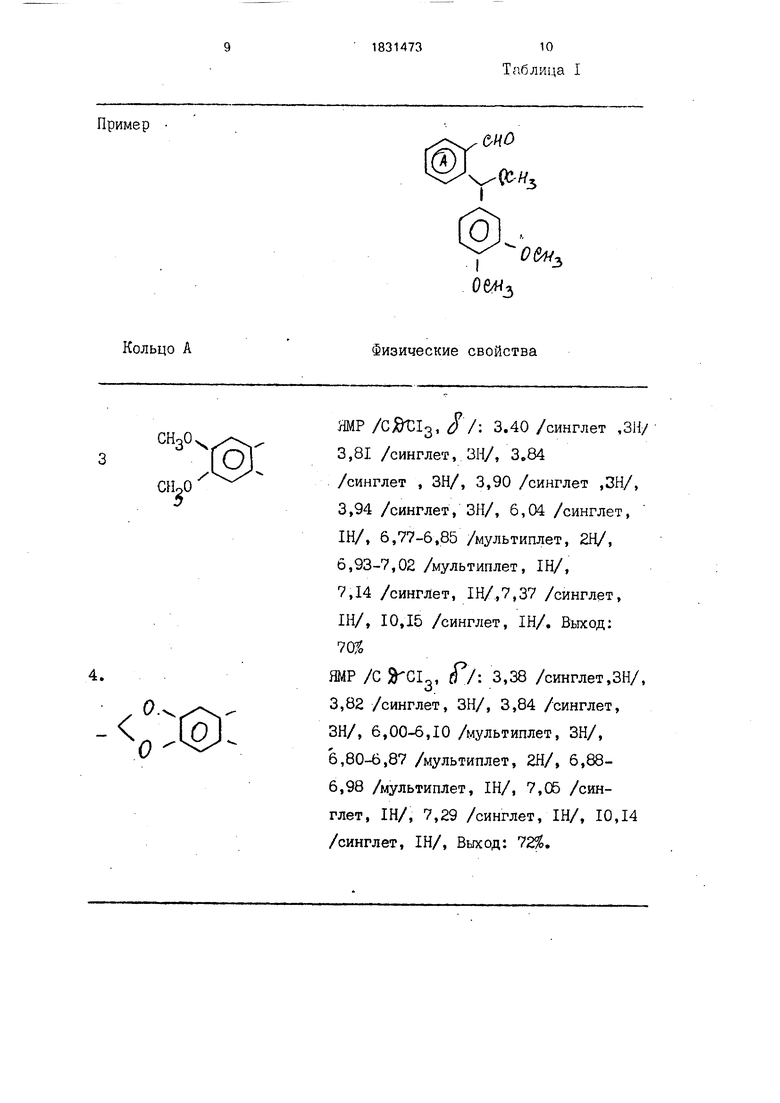
П р и м е р ы 3 и 4. Исходные соединения получают аналогично процедурам, описанным в примере 2.
Данные приведены в табл. 1.
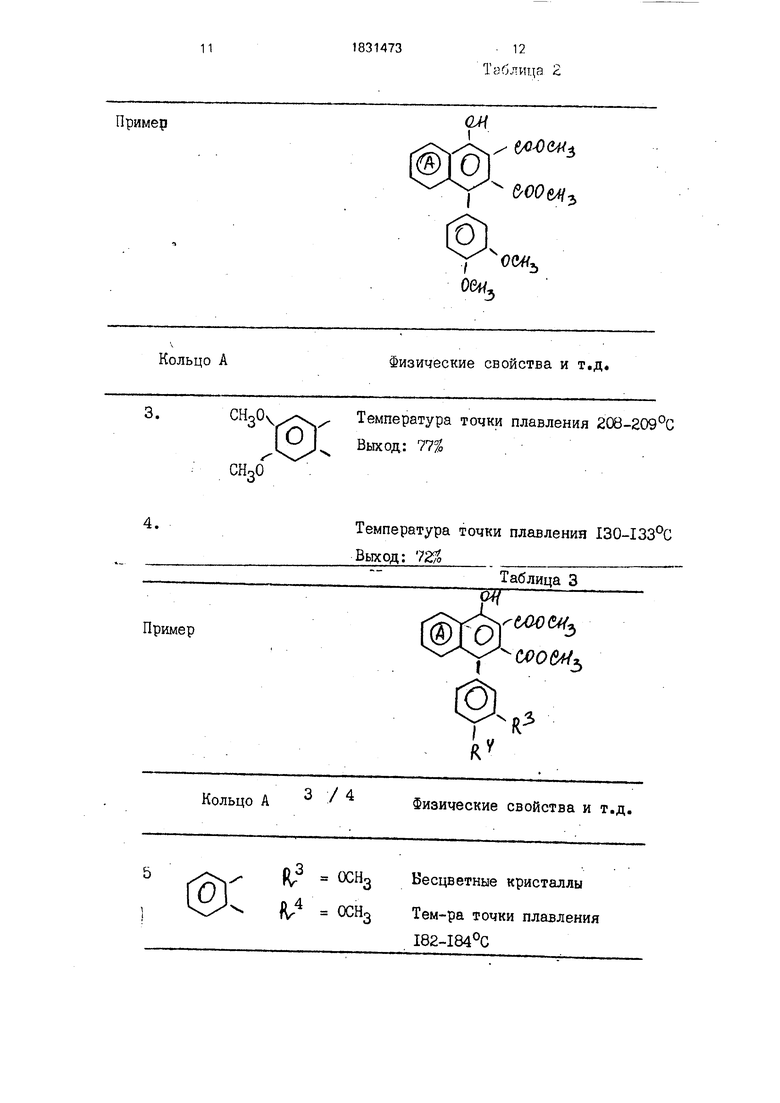
Исходные продукты, приведенные в табл,1, обрабатывают по той же схеме, что описана в примере 2. При этом получают соединения, перечисленные в табл.2.
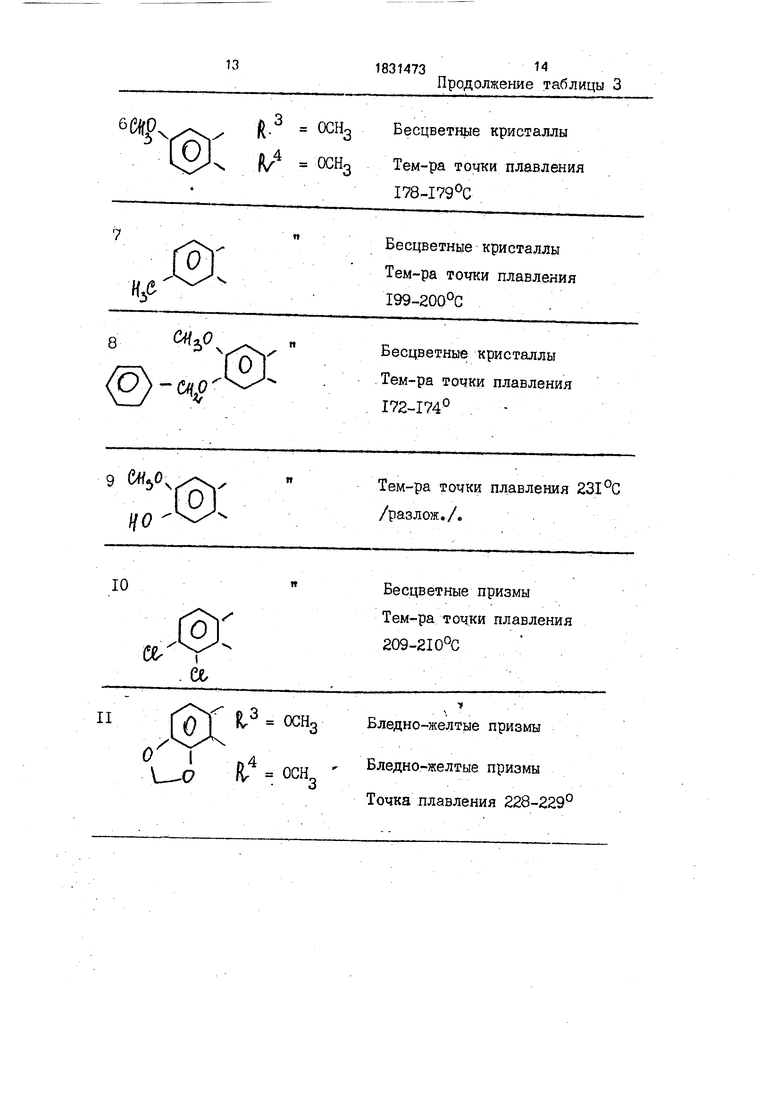
Пример 5-21. Соответствующие исходные соединения обрабатывают при помощи тех же процедур, что описаны либо в примере 1, либо в примере 2, в результате чего получают соединения, перечисленные в табл.3 и 4.
Формула изобретения
1. Способ получения производного нафталина общей формулы I ОНi
-COOR1
COOR2
где R1. R2 - низшая алкильная группа: R , R - низшая алкоксигруппа;
кольцо кольцо:
А - замещенное бензольное
R , R , R , R9, R10- низшая алкильная группа, или его фармацевтически приемлемой соли путем взаимодействия производного бензальдегида или его динизшего алкилаце- таля с низшим алкилацетилендикарбокси- латом формулы II
ОО
1 I
ROC-C5C-C--OR2
где RI, Ra имеют указанные значения, при нагревании до 60-80°С в присутствии кислоты, о т л и ч а ю щ и и с я тем, что, с целью упрощений процесса и повышения его селективности, в качестве производного бензальдегида используют производные общей формулы III:
OR5
где QR - низшая алкокси-Т1ли алканоилок- сигруппа.кольцо А;
R3, R имеют указанные значения, при этом в качестве кислоты используют низшую тригалоидалкановую кислоту и про- цесс проводят с использованием 1-2 экви- молярного количества карбоксилата по отношению к бензальдегиду, после чего полученный продукт при необходимости переводят в соль.
2. Способ по п. 1, о т л и ч а ю щ и и с я тем, что в качестве производного бензальдегида используют соединение формулы III, в котором кольцо А имеет формулы
где Re. Ra, Rio - имеют указанные значения.
1831473
10
Таблица I





Сущность изобретения. Продукт - производное нафталина общей формулы: ИЛИ Изобретение относится к новому способу получения производного нафталина, обладающего высокой гилолипидемической активностью, В частности, изобретение относится к производным 2-(3-и) или 4-низший алкокси- фенил-2,3-бис(низший алкоксикарбонил)-4- оксинафталина и.их солям. Цель заключается в упрощении процесса и повышении его селективности. R , R - низшая алкильная группа, R , R - низшая алкоксигруппа,кольцо А - замещенное бензольное кольцо v ROИЛИ R6. R7 58 R1D0 ,10 R°, R , R - низшая алкильная группа , или его фармацевтически приемлемой соли. Реагент 1: производное бензальдегида или его динизший алкилацеталь формулы ®с. сftb OR - низшая алкокси- или алканоилокси группа, кольцо A, R3, R -определены выше, Реагент 2: низший алкилацетилендикарбок- силат формулыQQ 1 IIII -, РОС-СнС-С-ОРГ R , R - указаны выше. Условия реакции: 60-80°С в присутствии низшей тригалои- далкановой кислоты с использованием 1- 2 эквимолярного количества карбоксилата по отношению к бензальдегиду. 1 з.п.ф-лы. 4 табл. Поставленная цель достигается за счет способа получения производного нафталина общей формулы: 9й «AS. е 00 CJ Ј VJ о (А
Пример
Кольцо А
сн3оч
СНоО
/
/°
,ю
ЯМР /С#С13, 8/ 3.40 /синглет ,ЗН/ 3,81 /синглет, ЗН/, 3.84 /синглет , ЗН/, 3,90 /синглет ,ЗН/, 3,94 /синглет, ЗН/, 6,04 /синглет, IH/, 6,77-6,85 /мультиплет, 2Н/, 6,93-7,02 /мультиплет, IH/, 7,14 /синглет, 1Н/,7,37 /синглет, IH/, 10,15 /синглет, IH/. Выход: 70Ј ЯМР /С Ј-CIQ, О: 3,38 /синглет,ЗН/,
о
3,82 /синглет, ЗН/, 3,84 /синглет, ЗН/, 6,00-6,10 /мультиплет, ЗН/, 6,80-6,87 /мультиплет, 2Н/, 6,88- 6,98 /мультиплет, IH/, 7,05 /синглет, IH/, 7,29 /синглет, IH/, 10,14 /синглет, IH/, Выход: 72.
&но
О&и
0№3
Физические свойства
11
Пример
Кольцо А
CHoOv
3 ;о
сн3о
Пример
Кольцо А
3/4
/
Ц3 - °сн3
ОСНо
1831473
12 Таблица Z
Ј0-0 MOvii
ося,
Физические свойства и т.д.
Температура точки плавления 208-209°С Выход: 77f0
Температура точки плавления 130-133°С Выход: 725Й
Таблица 3
Физические свойства и т.д.
Бесцветные кристаллы
Тем-pa точки плавления 182-184°С
7
№
9 Cf/Л
ЦО
10
s
се/
ее
II
о .
Кг ОСНоБледно-желтые призмы
У I
Л-о
I4 оси,
Бесцветные кристаллы Тем-pa точки плавления 199-200°С
Тем-pa точки плавления 231°С /разлож./.
Бесцветные призмы Тембра/точки плавления 209-210°С
Бледно-желтые призмы Точка плавления 228-229°
15183147316
Продолжение таблицы 3
о
12GO 2% Бесцветные кристаллы
с°х
Ш 1 002% Точка плавления 138-140°С
ое«3
о
«O-n-CgHr, Бесцветные иглы °С
и
. sO-n-CgHr, Точка плавления 132
14 3
fts 2% Бесцветные иглы
j 4 СЮН3Точка плавления 158°С
А О
15Л13 « ОСНо
V ... d
4
OCgHtj
о.
;:сот
Q , QCgHg Точка плавления 158-159°С
17& ОСН3v
V:
4 НТочка плавления 152-154°С
18уIt- « НБесцветные кристаллы
ОСН3 Точка плавления I69-I7I°C
Таблица 4
| АЛМАЗНАЯ БУРОВАЯ КОРОНКА | 0 |
|
SU267541A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Двухтактный двигатель внутреннего горения | 1924 |
|
SU1966A1 |
| БЫСТРОДЕЙСТВУЮЩИЙ КЛАПАН | 0 |
|
SU188248A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Пневматический водоподъемный аппарат-двигатель | 1917 |
|
SU1986A1 |
Авторы
Даты
1993-07-30—Публикация
1990-01-26—Подача