Изобретение относится к новым химическим соединениям, а именно, Н-производным 5-амино-6-меркаптопиримидина, обладающим противоопухолевым и цитбстатическим действием-, которые могут найти применение в медицине.
Наиболее близким по структуре и биологическим свойствам являются S-производные 5-амино-6-меркаптопиримндина, а именно дипиримидилсульфиды общей формулы
938553 , . . / левым и цитостатическим действием.
rj R - диметиламиногруппу, R метоксигруппу.
Соединения обладают противоопухо Описываемые соединения представляют собой устойчивые кристаллические вещества желтого цвета, растворимые в диметилформамиде, диметилсульфгде R и R - каждый метоксигруппа
(А) или R, - метоксигруппа, R - диметиламиногруппа (Б), отличающиеся от заявляемых соединений различным положением 5-нитропиримидинового остатка в молекуле.
Так, в известных соединениях (А и Б) указанный остаток находится при атоме серы, а в заявляемых соединениях (1а, б, в, г) - при атоме азота аминогруппы /
При изучении биологических свойст этих соединений установлено, что они проявляют относительно слабое цитостатическое действие и не обладают противоопухолевыми свойствами
Цель изобретения - расширение арсенала средств воздействия на живой организм, обладающих улучшенными, а также новыми биологическими свойствами, а именно цитостатическим и противоопухолевым действием соответственно.
Поставленная цель достигается Н-произБОдными .5-амино-6-меркаптопмгч|лммпм1- 3 rhonMVnbl
оксиде,
в водных и1елочах, плохо
растворимые в спиртах, эфире, бензоле, этилацетате, нерастворимые в вог де, т.пло 173-225°С.
Способ получения соединений общей формулы 1 основан на реакции внутримолекулярной перегруппировки Смайлса дигетерилсульфидов, протекающей при кипячении их в спирте.
Соединения формулы 1 получают взаимодействием соответствующего производного 5-амино-6-меркаптопиримидина обьчей формулы II
R .
SH
где R имеют вышеуказанные значения, с производным 5-нитро-6-хлорпиримидина об1цей формулы III
. , Е
где а) R и R кавдый означает метоксигруппу;,
б)R означает метокси-, R -диметиламиногруппу ;
в)R и R каждый означает диметиламиногруппу;
(Л.хН02
k.Ici
где R имеют вышеуказанные значения, в среде низшего спирта в присутствии щелочи при кипячений. Промежуточно 45 образующиеся дипиримидилсульфиды без выделения из реакционной массы претерпевают перегруппировку, превращаясь в соединения общей формулы I согласно схеме
т к
SH
R
Шг IJ GI
к
И R М Л
Ч- 3 Г
Нижеследующие примеры иллюстрируют способ полумения соединения б1дей формулы 1,
Пример 1 о Получение 4-метоки-5( -метокси-5 -нитропиримидил)-меркаптопиримидина (а),
К О.,6 г (3,1 моль) -метокси-5итро-6-хлорпиримидина в 0 мл метаола прибавляют 0,5 г (3,1 моль) kнитро-5 амино-6-меркаптопиримидинав 10 мл метанола и 0,17 г (3,1 моль) дкого кали. Смесь перемешивают при комнатной температуре 1 ч, потом кипятят tS мин, после чего охлаждат и выпавший осадок отфильтровыват и промывают водой.
1Ълучают 0,5 г продукта, упариванием фильтрата выделяют дополнительно 0,17 г в виде кристаллов желтого цвета с Топл 223-225°С (из этанола),
Общий выход 4-метокси-5 ( -метокси-5 -нитропиримидил-6 )-амино-6меркаптопиримидина составляет 75%
Найдено,%; С 38,52; Н 3,46; N 27,08; S 10,28
С,оН,
Вычислено,: С 38,70; Н 3,24; N 27,08; S 10,33
HK-cneKTp,-N)cM : 330 (N1-1)
УЛ спектр, длпу;,с в ммк (Е.); 300 ()o
П р и м е р 2, Получение -метокси-5 Ct -диметиламино-5-нитропиримидил-) )-амино-6-меркаптопиримидина,
В условиях примера 1 из 0,65 г 3,1 ммоль) А-диметиламино-З-нитро-бхлорпиримидина и 0,5 г (3,1 ммоль) 4-метокси-5-амино-6-меркаптопиримидина получают 0, г ( -метокси-5(k -лиметиламино-5 -нитропиримидил6 )-амино-Г1-меркаптопиримидина в виде желтого кристаллического порошка, т.пл, 173 175°С (из этанола).
Найдено,%: С 40,94; Н 4,24; , ., N 30,08.
С„11,
Вычислено, С 40,86; Н 4,03; N 30,32, ,
938553
R Н
нХ. L 1
SH т
ИК-спектр, ЗЗПО (NH) УФ-спектр, )д, в .ммк (): 305 (11100),
ПримерЗо Получение -диметиламино-5- (k-диметиламино-5-нитропиримидил-6)-амино-б-меркаптопиримидина.
В условиях примера 1 из 0,58 г (3,1 жoль) +-диметиламино-5 НитрО 6-хлорпиримидина и 0,5 г (3,1 ммоль) -диметиламино-5-амино-б-меркапто. пиримидина получают 0,0 г (G0%) kдиметиламино-5-С -диметиламино-5 нитропиримидил-6 )-амино-6-меркаптопиримидина в виде желтого кристаллического порошка, Топл, 190-192 С (из этанола),
Найдено,%: С 42,83; Н 4,82, С-, S
Вычислено,: С 42,85; Н 4,79, ИК-спектр, ) 32бО (МП) УФ-спектр,. ммк (): 266 , 5 (27600); 310 (19500)о
Примерно Получение -диметиламино-5-(-метокси-5 -нитропиримидил-6 )-амино-6-меркаптопиримидмна,
0 В условиях примера 1 из 0, г (3,° ммоль) -метокси-5 нитро-6-хлорпиримидина и 0,6 г (3,В ммоль) диметиламино-5-амино-6-меркаптопиримидина получают 0,96 г (Г-0%) -ди5 метиламино-5-( -метокси-5-нитропиримидил-6 ) -амино-6-меркаптопиримидина в виде желтого кристаллического порошка, ТоПЛо 177-17В С (из этанола)а .
0 Найдено,%: С 40,97; Н 4,09; N 30,42; S 10,15.
Вычислено,%: С 40,86; Н 4,03; N 30,32; S 9,9 5 ИК-спектр, V см : 3250 (Nil)
УФ-спектр, (22200); 31 (1Я600),
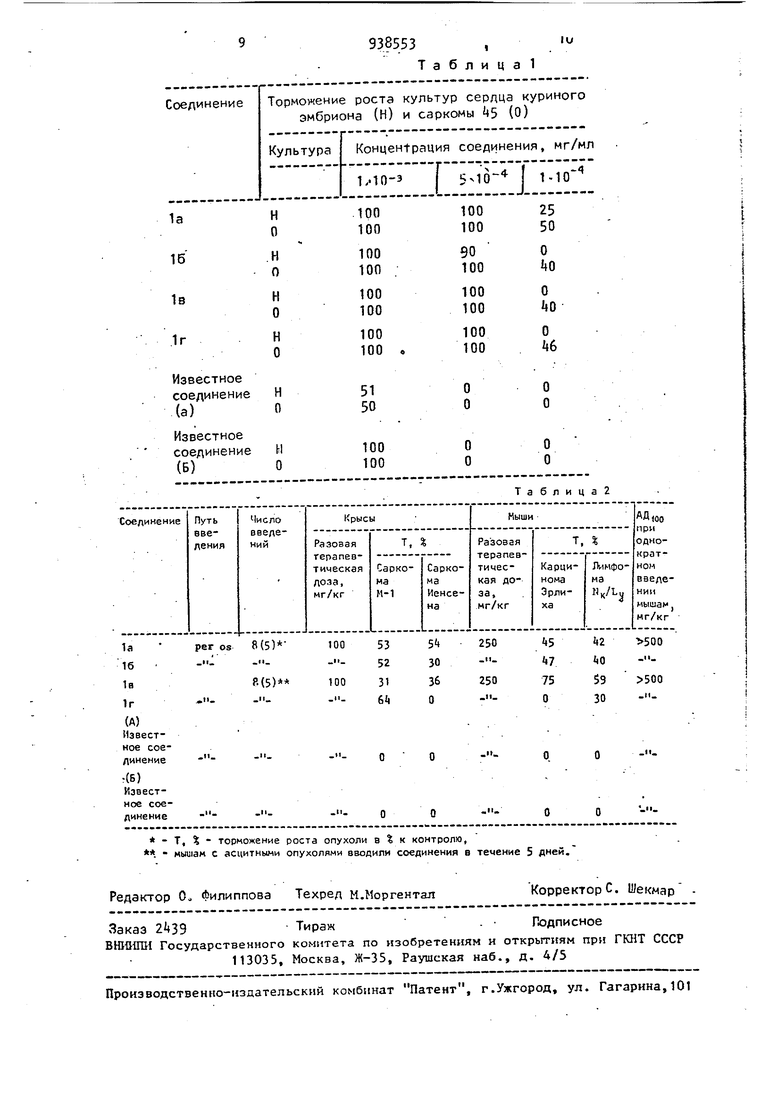
Исследование биологической актио. ности. 7 Копичественная характеристика би логической активности заявляемых со динений, а)Цитостатическое лействие„ Иитостатическое действие соединений об111ей формулы 1 изучали in vitro в первичных культурах нормальной (сердце куриного эмбриона) и опухолевой (саркома 5) тканей, Оценку действия соединений проводили после 72 или 9б-ти часовой инку бации с веьчеством при , Индекс торможения роста культур вычисляли по принятой методике Сравнительные данные исследования цитостатического действия предлагаемых и известных соединений пред ставлены в таблЛо Как видно из экспериментальных данных, представленных в табл.Т, все соединения в концентрации 1 ЮЗ и БПО мг/мя подавляют рост нормаль ной и опухолевой тканей на ЭО-ЮО, в концентрации IlO вызывают тормо жение в основном только опухолевой ткани, в то время как известные сое динения А и В оказывают действие на рост нормальной и опухолевой тканей лишь а высокой концентрации (1 ХЮЗ мг/мл). Таким образом, цитостатическое действие заявляемых соединений значительно выше, чем у известных анал гов А и Б. Кроне того, соединения 1 б, в, г обладают избирательностью действия на опухолевую ткань. б)Противоопухолевая активность, Изучение активности соединений общей 1юрмулы 1 проведено в опытах in vivo на 53б крысах и мышах с пер виваемыми опухолями - саркомой Иенс -8 на и саркомой М-1 крыс, карциномой Эрлиха и лимфомой мышей. Для сравнительной оценки изменения веса опухоли (Т, %) по сравнению с контрольной, животным леченной группы вводили заявляемые соединения per OS 3 виде суспензии в подсолнечном масле 1 раз в день в течение В дней - для солидных опухолей, и в течение 5 дней - для асцитныхо Сравнительные результаты исследо,вания противоопухолевой активности и токсичности предлагаемых и известных соединений приведены в табл.2, Как видно из данных таблицы, соединения 1 а-г при введении в терапевтической дозе тормозят рост саркомы Н-1 и Иенсена крыс ,на ЗО-б и тормозят развитие карциномы ; Эрлиха и лимфомы N,/L мышей на При.исследовании -изве.стных соединений А и Б в тех ке условиях противоопухолевая активность не обнаруже - на. .. Токсичность заявляемых соединений. Как видно из данных табл., заявляемые соединения нетоксичныо Летальная доза, вызываю1чая гибель 100 животных (ЛЛ.1оо) при однократном введении 500 мг/кг С ЗСравнительное биологическое изучение показало, что описываемые соединения (соединения а-г) существенно превосходят известные соединения А и Б по цитостатическому действию и проявляют избирательность действий на противоопухолевую ткань. Кроме того, заявляемые соединения, в отличие от известных обладают новым свойством - противоопухолевой активностью.
938553,
lU
Таблица 1



| название | год | авторы | номер документа |
|---|---|---|---|
| S-Производные 5-амино-6-меркаптопиримидина, обладающие противоопухолевым и цитостатическим действием | 1980 |
|
SU938559A1 |
| Производные дипиримидо [(4,5 - @ )(5,4 - @ )]-(1,4)тиазинов и способ их получения | 1975 |
|
SU550829A1 |
| Производные 6Н-7,8-дигидропиримидо [4,5-B] [1,4]бензтиазина и способ их получения | 1979 |
|
SU811776A1 |
| Производные пиримидо (4,5- @ ) (1,4) бензтиазепина и способ их получения | 1977 |
|
SU677355A1 |
| 4,9-Бис-аминопроизводные дипиримидо-5Н-(4,5-В)-(4 @ ,5 @ - @ )-(1,4)тиазина, обладающие цитостатическим противоопухолевым и антиредуктазным действием | 1982 |
|
SU1085204A1 |
| БРОМГИДРАТ 4-МЕТОКСИ-7,7-ДИМЕТИЛ-9(5'-КАРБОКСИАМИЛ)АМИНО-6Н-7,8-ДИГИДРОПИРИМИДО(4,5-b)-1,4-БЕНЗТИАЗИН И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2008 |
|
RU2387658C1 |
| ГИДРОХЛОРИДЫ СЕРОСОДЕРЖАЩИХ 2-АМИНОИМИДАЗОЛОВ ИЛИ 2-АМИНОТИАЗОЛОВ, ОБЛАДАЮЩИЕ ЦИТОТОКСИЧЕСКОЙ И ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ И ПРОЯВЛЯЮЩИЕ ИНГИБИРУЮЩЕЕ ДЕЙСТВИЕ В ОТНОШЕНИИ НЕКОТОРЫХ ФЕРМЕНТОВ | 1995 |
|
RU2076864C1 |
| N -ФОСФОРИЛИРОВАННЫЕ ПРОИЗВОДНЫЕ 3- β -ФЕНИЛИЗОПРОПИЛСИДНОНИМИНА, ОБЛАДАЮЩИЕ ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 1991 |
|
RU2036914C1 |
| Производные 6,7,8,9-тетрагидродипиримидо-(4,5- @ ) (5,4- @ ) (1,4) тиазина или 6,7,8,9,-тетрагидропиридо (2,3- @ ) пиримидо (4,5- @ )-(1,4) тиазина и способ их получения | 1975 |
|
SU551873A1 |
| Производные пиримидо (5,4- @ ) изохинолина и способ их получения | 1978 |
|
SU725427A1 |
N-производные 5-амино-б-меркап - топиримидина общей формулы 1 R N где R и К означают каждый метоксигруппу или R - метоксигруппу, R - диме тиламиногруппу, или R и R - каждый означает диметилсл аминогруппу, или R - диметиламино-, R- метоксигруппу, обладающие противоопухолевым и цитостатическим деиствиемо о со 00 СП ел W 
| Производные дипиримидо [(4,5 - @ )(5,4 - @ )]-(1,4)тиазинов и способ их получения | 1975 |
|
SU550829A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Osknr Ко Rodig, Richard Е, Collier, Robert К„ Schlatzer, The Smiles Rearraup,etnent of the 3-/jnino-2,2 - . | |||
| dipyridyl sulfide system, J Org chem | |||
| Прибор для заливки свинцом стыковых рельсовых зазоров | 1925 |
|
SU1964A1 |
| Способ обработки угля | 1923 |
|
SU2652A1 |
| Методы экспериментальной хямиотерапрш Под ред | |||
| ГоН | |||
| Першина, И,: Медицина, 1971, с | |||
| Клапан | 1919 |
|
SU357A1 |
| Неотложна я помощь при острых отравлениях (справочник по токсикологии,под редакцией акад | |||
| АМН СССР Л.Н | |||
| Голикова ), N.: Медицина, 197П, с | |||
| Способ изготовления фасонных резцов для зуборезных фрез | 1921 |
|
SU318A1 |
Авторы
Даты
1992-05-23—Публикация
1980-12-12—Подача