Изобретение касается каталитической системы, состоящей из катализатора A и сокатализатора B, для гомополимеризации этилена или сополимеризации этилена с одним или более α-олефинов, состоящих из 3-12 атомов углерода, и по желанию, с одним или более неконъюгированных диенов, причем катализатор A состоит из одного или более магнийорганических соединений, галогенида и одного или более соединений переходного металла. Это изобретение также касается получения каталитической системы и сополимеризации этилена с помощью каталитической системы.
Каталитическая система этого типа описана в NL-A-7605544. Галогенид, который используется в этой системе, однако, спонтанно реагирует с магнийорганическим(и) соединением(ями). "Реагирует спонтанно" означает, что тонко диспергированный нерастворимый материал образуется, когда галогенид добавляется к магнийорганическому соединению, растворенному в подходящем растворителе при комнатной температуре и при атмосферном давлении. В примерах NL-A-7605544 приведено использование, в частности, HCl, который является высоко коррозийным газом, со всеми вытекающими последствиями. Кроме того, третичный бутилхлорид также использован в примерах. Недостаток третичных хлоридов состоит в присущей им реактивности. Это приводит к реакциям, которые труднее контролировать при получении катализатора.
Цель этого изобретения состоит в получении каталитической системы, которая не дает вышеупомянутых недостатков, и которая, кроме того, проявляет очень высокую активность при высоких температурах и коротком времени обработки в реакторе для полимеризации с высокой степенью конверсии сомономера. Более того, эта каталитическая система может быть получена простым и регулируемым способом.
Эта цель достигается тем, что галогенид является органическим хлоридом, который не реагирует спонтанно с магнийорганическими соединениями, и тем, что каталитическая система также содержит по крайней мере один агент переноса.
Здесь и здесь далее агентом переноса является соединение, которое способно к переносу к магнийорганическому соединению атома хлора из органического хлорида, который не реагирует спонтанно с магнийорганическим соединением. "Не реагирует спонтанно"" означает, что не образуется никакого тонко диспергированного нерастворимого материала, когда хлорид добавляется к магнийорганическому соединению, растворенному в подходящем растворителе при комнатной температуре и при атмосферном давлении.
Каталитическая система по этому изобретению обладает, кроме того, очень хорошим сочетанием свойств. Она проявляет высокую активность при высоких температурах полимеризации, степень превращения сомономера очень хорошая и молекулярный вес и распределение молекулярного веса полиэтилена можно регулировать, что очень важно. Широкое распределение молекулярного веса приводит к хорошим реологическим свойствам при высоких скоростях сдвига, другими словами, к хорошей технологичности. Узкое распределение молекулярного веса по существу приводит к худшей технологичности, но лучшим механическим свойствам полимера. Каталитическая система по этому изобретению и ее получение недороги и оказывают наименьшее возможное влияние на окружающую среду. Кроме того, полиэтилен, который производится с помощью каталитической системы по этому изобретению, имеет очень низкие остаточные концентрации галогена и переходного металла. Остаточные концентрации других металлов, например, из катализатора B и агента переноса, очень низки.
Уже существуют многочисленные каталитические системы, которые способны к полимеризации этилена и/или 1-алкенов. Такая полимеризация происходит в газовой фазе, в растворе, в пульпе, в ядре или в суспензии. В растворе и в суспензии полимеризация происходит в растворителе или диспергирующем веществе, соответственно. Если этилен полимеризуется в растворе, температура полимеризации находится выше температуры растворения полиэтилена. В суспензии, напротив, полимеризация происходит при температуре ниже температуры растворения образуемого полиэтилена. В основном, катализаторы, которые подходят для полимеризации в пульпе, газовой фазе, в массе и суспензии, не подходят для полимеризации в растворе.
Полимеризация в растворе чрезвычайно удобна, если необходим процесс полимеризации, который делает возможным быстрые изменения качества продукта, которые нужно выполнить. Это процесс с большими возможностями к изменению. Эта гибкость происходит благодаря короткому времени обработки продукта в реакторе, в то же время, тем не менее, может быть произведен полиэтилен хорошего качества.
В течение долгого времени существует потребность в каталитических системах, которые могут полимеризовать при высоких температурах, что дает несколько преимуществ. Полимеризация этилена является экзотермической реакцией. Это создает проблему отвода тепла полимеризации. Одним из возможных ее решений конечно является охлаждение через стенки или с помощью охлаждающих устройств в реакторе. Это может, однако, приводить к отложению полимера на охлаждающих поверхностях, особенно когда температура охлаждения ниже температуры плавления полиэтилена. Чтобы избежать этой проблемы отложения, возможно также в основном охлаждать питание реактора, однако, для этого требуется много энергии. Если полимеризация проводится при высокой температуре, охлаждение питания реактора может быть снижено или даже отключено, в то же время, тем не менее, может быть получена высокая степень превращения этилена с помощью каталитической системы по данному изобретению, другими словами, каталитическая система обладает высокой активностью. Более того, меньшее дополнительное нагревание будет затем необходимо или совсем не нужно для испарения растворителя при дальнейшей обработке полимера.
Высокотемпературные каталитические системы должны быть так активны, чтобы они все еще проявляли достаточную активность при температурах полимеризации, равных 150oC и выше. Проблема, с которой сталкиваются при полимеризации при таких высоких температурах, состоит в продукции полимеров с достаточно высоким молекулярным весом.
Органические хлориды, которые используются в каталитических системах по этому изобретению, являются хлоридами, которые не реагируют спонтанно с магнийорганическим(и) соединением(ями). Органические хлориды являются первичными и/или вторичными моно-, ди- или поли-(хлор) замещенными алкилами, алкенилами, арилами или алкарилхлоридами или их смесями. Алкильная, алкенильная, арильная или алкарильная группа может содержать 1-20 атомов углерода. Под поли(хлорид) замещенным соединением понимается соединение с двумя или более атомами хлора, причем атомы хлора помещены у одного или более атомов углерода.
Органический хлорид может также быть цикло- или полициклоалкил-, алкенил-, арил- или алкарилсоединением с 5-20 атомами углерода. С полициклосоединением это означает соединение, которое содержит 2 или более циклических структур, причем эти циклические структуры могут быть в прямом контакте друг с другом, или каждое может быть отделено от другого одним или более атомов углерода.
Первичный органический хлорид предпочтительно выбирается из группы, состоящей из 1-хлорбутана, 1-хлорпропана, хлорэтана или их смеси.
Вторичный органический хлорид предпочтительно выбирается из группы, состоящей из 2-хлоргептана, 3-хлоргептана, 2-хлорбутана, 2-хлорпропана или их смеси.
Может также использоваться, например, смесь одного или более первичных и одного или более вторичных органических хлоридов. Примерами таких смесей являются, например, 1-хлорбутан/2-хлорбутан или 1-хлордекан/2-хлорбутан. Органические хлориды смеси могут использоваться одновременно или поочередно. Отношение между органическими хлоридами в этих смесях может меняться в широких пределах, и наилучшее отношение может быть легко определено специалистом. Наилучший порядок, в котором используются органические хлориды, может быть легко определен.
Поли-(хлорид) замещенное соединение может, например, быть 2,2-дихлорбутаном, 2,2-дихлорпропаном, 1,3-дихлорбутаном, 1,2-дихлорбутаном или 1,2-дихлорпропаном.
Цикло- или полициклосоединение может быть циклопентилхлоридом или, например, хлорбензолом.
В качестве агента переноса, например, может использоваться одно или более алюминийорганических соединений и/или одно или более борорганических хлоридов и/или одно или более цинкорганических соединений. В качестве хлорида бора, например, может использоваться трихлорид бора. Соединение цинка может, например, выбираться из диэтилцинка или дихлорида цинка.
Предпочтительно, агентом переноса является хлорид алюминийорганического соединения. Более предпочтительно, чтобы хлорид алюминийорганического соединения выбирался из группы, состоящей из алюминия трихлорида, этилалюминия дихлорида, диэтилалюминия хлорида, сесквиэтилалюминия хлорида или их смеси.
В качестве магнийорганического соединения особенно подходит диалкилмагниевое соединение. Однако также могут использоваться алкилалкоксимагниевое соединение или диалкоксимагниевое соединение. Магнийорганическое соединение может быть представлено общей формулой R1R2Mg, в котором R1 и R2 могут быть одинаковыми или разными и представлять собой алкильные или алкоксильные группы из 1-20 атомов углерода. Предпочтительно, чтобы магнийорганическое соединение растворялось в углеводородах.
Примерами магнийорганических соединений являются ди(н-бутил) магний, н-бутил-сек-бутилмагний, диизопропилмагний, ди(н-гексил)магний, изопропил-н-бутилмагний, этил-н-гексилмагний, этил-н-бутилмагний, ди(н-октил)магний, бутилоктилмагний, диэтоксимагний, дибутоксимагний, бутоксиэтоксимагний.
Предпочтительно используются этилбутилмагний, бутилоктилмагний, дибутилмагний и/или дигексилмагний, которые могут превращаться или нет с помощью по крайней мере двух молярных эквивалентов спирта, по отношению к магнию, в алкилалкоксимагниевое соединение, диалкоксимагниевое соединение или смесь таких соединений.
Если используется магнийорганическое соединение, которое растворимо в углеводородах, можно также использовать комплексы магнийорганического соединения с алюминием, такие как ди(н-бутил)магний•1,6-триэтилалюминий. Возможны также комплексы с эфиром. Конечно, также возможны смеси этих соединений.
В качестве соединения переходного металла можно использовать соединения Ti, V, Zr, Hf или смесь этих соединений.
В качестве соединений переходного металла могут использоваться соединения как трехвалентного, так и четырехвалентного титана. Эти титановые соединения имеют общую формулу Ti(OR1)4-nXn 1 или Ti(OR2)3-mXm 2, где R1 и R2 могут быть одинаковыми или разными и представлять собой углеводородные радикалы, имеющие 1-20 атомов углерода, и X1 и X2 галогеновыми атомами, 0 ≤ n ≤ 4 и 0 ≤ m ≤ 3. Также с успехом может быть использована смесь соединений четырехвалентного и трехвалентного титана.
Предпочтительно использовать эфир титановой кислоты, например, тетрабутоксититан (ТБТ), для наибольшего повышения активности. Однако четыреххлористый титан также дает хорошие результаты. Конечно, также возможна комбинация ТБТ и TiCl4. Также могут использоваться титановые комплексы, такие как TiCl3•3-деканол, TiCl3•3-тетрагидрофуран, TiCl3•3-пиридин. Примерами других соединений переходных металлов являются VCl4, VOCl3, ZrCl4, Zr(OiPr)4, Zr(OBu)4 и HfCl4.
Молярное отношение хлорида из органического хлорида и магния из магнийорганического соединения находится между 1 и 10, предпочтительно, между 1,5 и 5, и в особенности, между 1,5 и 3.
Молярное отношение металла из агента переноса и магния из магнийорганического соединения находится в интервале между 0,01 и 2, предпочтительно, между 0,1 и 1,5, и в особенности, между 0,1 и 1.
Молярное отношение магния из магнийорганического соединения и переходного металла в основном находится между 1 и 100, предпочтительно, между 3 и 50, и в особенности, между 4 и 20.
Каталитическая система может быть изготовлена следующим образом. Магнийорганическое соединение растворяют в углеводороде. Подходящими углеводородами являются пентан, гептан, бензин и т.д. Органический хлорид дозируется по отношению к магнийорганическому соединению, содержащему углеводород. Затем по каплям добавляется агент переноса. Полученную смесь затем перемешивают в течение определенного отрезка времени, который может изменяться в пределах от примерно 10 секунд до нескольких часов, и нагревают при температуре от 20oC до точки кипения углеводорода, по желанию, под давлением. Затем добавляют соединение переходного металла, и реакционную смесь снова нагревают при температуре от комнатной температуры до точки кипения углеводорода при перемешивании в течение определенного отрезка времени, который может изменяться от примерно 10 секунд до нескольких часов. Каталитическая система не должна отделяться посредством фильтрации или декантации и ее не нужно промывать эфиром. Другой возможный способ приготовления состоит в растворении агента переноса в углеводороде, куда добавляется смесь магнийорганического соединения, углеводорода и органического хлорида. В остальном способ получения остается таким же, что и описанный выше. Предпочтительно используется этот последний способ, так как по этому способу реакцию можно очень хорошо регулировать.
Как уже упомянуто выше, использование такого органического хлорида в сочетании с агентом переноса устраняет необходимость отделять каталитическую систему посредством фильтрации или декантирования и отмывать ее, и тем не менее остаточные количества хлора и титана в полиэтилене очень низки, конечно, в сравнении с общепринятой каталитической системой, такой, например, как описанная в EP-A-126515.
В случае каталитической системы, описанной в EP-A-126515, такие остаточные количества, которые получены с помощью каталитической системы по этому изобретению, нельзя получить без отмывания. В EP-A-126515 необходим избыток алкилалюминийхлорида для хлорирования магнийорганического соединения. Это значит, что или избыток алкилалюминийхлорида должен быть отмыт, или содержание хлора в полиэтилене будет высоким. Если присутствует стадия отмывания при приготовлении катализатора, получаются содержащие хлор отходы, которые, конечно, очень нежелательны для окружающей среды. Недостаток присутствия больших количеств хлора в полимере состоит в том, что технологическое оборудование подвергается коррозии, и что необходимы относительно большие концентрации ингибитора коррозии. С помощью каталитической системы по этому изобретению получается полиэтилен с очень низкими остаточными концентрациями хлора, несмотря на то, что нет необходимости отмывать каталитическую систему, что означает, что также не продуцируется никаких отходов.
Предполагается, что реакция происходит следующим образом. В каталитической системе по этому изобретению используется органический хлорид, который спонтанно не реагирует с магнийорганическим соединением. Если агентом переноса является, например, сесквиэтилалюминийхлорид (СЭАХ), предполагается следующий механизм. Хлор переносится с алюминия на магний, и в то же время магний передает углеводородную группу R алюминию, так что образуются связи Mg-Cl (и связи R-Al) и в конечном счете "MgCl2". Тем временем органический хлорид (R'-Cl) реагирует с образовавшимся R-Al с получением новых связей Al-Cl, которые могут в свою очередь реагировать со связями R-Mg. Таким образом, магнийорганическое соединение хлорируется, в этом случае, СЭАХ, в то время как достаточна небольшая доза СЭАХ. Для того, чтобы было возможно хлорирование магнийорганического соединения до "MgCl2" при общепринятом способе получения катализатора необходим избыток СЭАХ, как, например, описано в EP-A-126515. Это можно объяснить на основе того факта, что СЭАХ не отдает весь свой хлор магнию. Если магнийорганическое соединение должно хлорироваться, например, с помощью СЭАХ при молярном соотношении СЭАХ/R2Mg, равном 0,5, это означает, что существует стехиометрический дефицит хлора (Cl/Mg = 0,75, тогда как требуется Cl/Mg ≥ 2). Даже если СЭАХ должен был отдать весь свой Cl (что с этих пор не так), количественное образование "MgCl2" (более или менее) все же не должно быть возможно. Большая часть хлора из "MgCl2", образовавшегося в каталитической системе по данному изобретению должна, следовательно, поступать из органического хлорида. Термин "агент переноса" был сформулирован на основании вышеизложенной гипотезы по действию, например, СЭАХ. Хотя эта гипотеза предоставляет объяснение для наблюдаемого хлорирования, нельзя исключить возможность совсем другого механизма.
Изобретение при этом не ограничивается какой-либо теорией относительно существующего механизма.
В дополнение к катализатору A, описанному выше, каталитическая система, кроме того, включает сокатализатор B или смесь сокатализаторов. Цель этого состоит в том, чтобы сделать возможным повышение активности системы, и следовательно, выход полиэтилена в процессе полимеризации и даже потом. Примерами таких сокатализаторов B являются металлоорганические соединения, содержащие металл из группы 1, 2 или 13 Периодической системы элементов, которые можно найти в "CRC Handbook of Chemistry and Physics", 70-е издание, 1989-1990. Предпочтительно, используется алюминийорганическое соединение, примерами алюминийорганических соединений являются триэтилалюминий (ТЭА), триизобутилалюминий (ТИБА), триоктилалюминий (ТОА), триизопренилалюминий (ипренил)3Al, диэтилалюминийхлорид (СЭАХ), сесквиэтилалюминийхлорид (СЭАХ), диэтилалюминия гидрид (ДЭАГ), диэтилалюминия оксид (ДЭАОК), метилалюминоксан (МАО), или очень подходят их смеси. Предпочтительны ТЭА и ДЭАХ.
Катализатор A и сокатализатор B можно добавлять в реактор для полимеризации отдельно или в сочетании.
Молярное отношение агента переноса из катализатора A и сокатализатора B находится в пределах между 0,003:1 и 20:1, предпочтительно, между 0,04:1 и 5:1.
Также возможно дополнительно дозировать один или более органических хлоридов, которые не реагируют спонтанно с магнийорганическим(и) соединением(ями) в реакторе для полимеризации. Это может привести к дополнительному увеличению активности.
Изобретение, кроме того, касается процесса гомо- или сополимеризации этилена с одним или более α-олефинов, имеющих 3-12 атомов углерода, и, произвольно, одним или более неконъюгированными к полиэтилену диенами. α-олефинами, которые особенно подходят, являются пропилен, 1-бутилен, 1-гексен и 1-октен. Известно, что включение сомономера приводит к увеличению прочности полиэтилена. Чем выше α-олефин, тем больше прочность, что означает следующую последовательность: 1-бутилен < 1-гексен < 1-октен. То же справедливо и для химической устойчивости, что также называется трещиностойкостью при внешней нагрузке (ТСВН).
Примерами подходящих диенов являются 1,7-октадиен и 1,9-декадиен.
Каталитическая система по этому изобретению может в принципе применяться при полимеризации в газовой фазе, суспензии, растворе или полимеризации в массе. Однако было обнаружено, что каталитическая система данного изобретения особенно подходит для полимеризации в растворе этилена при высоких температурах, свыше 150oC. Предпочтительно, полимеризация осуществляется при температуре свыше 165oC. Обычно температура полимеризации не превышает 250oC. Полученный полиэтилен имеет в принципе очень низкое содержание хлора и титана, которое означает, что нет необходимости в удалении остатка катализатора.
Любая жидкость, которая является инертной в отношении каталитической системы, может использоваться в качестве диспергирующего средства, как при приготовлении катализатора, так и при реакции полимеризации. Пригодны один или более насыщенных, неразветвленных или разветвленных алифатических углеводородов, таких как бутаны, пентаны, гексаны, гептаны, пентаметилгептан или фракции нефти, такие как легкий или обыкновенный бензин, тяжелый бензин, керосин или газойль. Пригодны ароматические углеводороды, такие как бензол или толуол, но из-за высокой стоимости, а также по соображениям безопасности такие растворители, предпочтительно, нежелательно использовать при производстве в промышленном масштабе. Поэтому при полимеризации промышленного масштаба нужно предпочтительно использовать в качестве растворителя дешевые алифатические углеводороды или их смеси, такие как те, что продаются нефтехимической промышленностью. Сушка или очистка желательны в случае таких растворителей; они могут быть осуществлены без проблем специалистом среднего уровня.
Раствор полимера, полученный при полимеризации, может быть обработан известным способом. В основном катализатор дезактивируется на той же стадии при дальнейшей обработке полимера. Эта дезактивация также осуществляется известным способом. Удаление остаточного катализатора из полимера может не производиться вследствие того, что количество катализатора в полимере, в частности, концентрация хлора и переходного металла теперь очень низка в результате использования каталитической системы по этому изобретению.
Полимеризация может осуществляться при атмосферном давлении, но также и при повышенном давлении до 300 МПа непрерывным и не непрерывным способом. Если полимеризация проводится под давлением, выход полимера может быть повышен еще больше, что дает в результате даже более низкое содержание остаточного катализатора. Полимеризация, предпочтительно, осуществляется при давлении от 0,1 до 25 МПа, конкретно, от 1 до 15 МПа. Давление, равное 100 МПа или выше, может применяться, если полимеризация проводится в так называемых реакторах высокого давления. Катализатор по данному изобретению может также успешно применяться при процессе при высоком давлении.
Молекулярный вес полимера можно регулировать обычным образом путем добавления водорода или других регуляторов длины цепи, например, цинкалкильных соединений.
Полимеризацию можно также проводить в несколько стадий как последовательно, так и параллельно. На этих различных стадиях состав катализатора, температура, концентрация водорода, давление, время обработки и т.д. можно произвольно изменять. Таким образом могут быть также получены продукты с широким распределением по молекулярному весу.
Данное изобретение будет объяснено в следующих примерах без ограничения его этим. Примеры иллюстрируют высокую продуктивность при коротком времени обработки и высокой температуре в реакторе для получения полиэтилена с высоким молекулярным весом. Плотность (d) определяли по стандарту ASTM D792-66. Показатель плавления (M. I. = ПП) определяли по стандарту ASTM D1238, положение Е. Отношение течения расплава (MFR = ОТР) представляет собой I21,6/I2,16, где I21,6 определяется по стандарту ASTM D1238, а I2,16 определяли по стандарту ASTM D1238, положение E. Это использовано здесь в качестве меры распределения по молекулярному весу.
Пример 1
Получение катализатора
Весь процесс получения проводили с исключением воздуха и влаги и в инертной азотной атмосфере. Все реакции проводили при перемешивании с помощью стеклянной мешалки.
100 мл бензина вводили в стеклянную колбу. К этому в качестве агента переноса добавляли 2,85 мл сесквиэтилалюминийхлорида (СЭАХ, полученного от Witco). Затем готовили смесь 50 мл бензина, 50 мл 20%-ного раствора бутилоктилмагния в гептане (BOMAG-A®, полученного от Witco) и 9,1 мл изопропилхлорида. Это была прозрачная бесцветная жидкость. Затем в течение двухчасового промежутка времени эту смесь по каплям добавляли при комнатной температуре и при перемешивании к раствору СЭАХ в бензине. Образовывался осадок. После того, как был добавлен весь BOMAG-A®, полученную смесь перемешивали при комнатной температуре в течение 3,5 часов. Затем к этой смеси по каплям в течение 0,5 часа добавляли 1,71 мл тетрабутоксититана (ТБТ) в 50 мл бензина. После того, как раствор ТБТ добавлен, всю смесь перемешивали при комнатной температуре в течение двух часов.
Пример 2
Получение катализатора A
Получение, как описано в примере 1, с использованием 10,4 мл 1-хлорбутана вместо изопропилхлорида.
Пример 3
Получение катализатора A
Получение, как описано в примере 1, с использованием 10,6 мл 2-хлорбутана вместо изопропилхлорида.
Пример 4
Получение катализатора A
Получение, как описано в примере 3, но теперь в качестве агента переноса использовали 1,24 мл диэтилалюминийхлорила (ДЭАХ).
Пример 5
Получение катализатора A
Получение, как описано в примере 3, но теперь использовали 0,28 мл СЭАХ.
Пример 6
Получение катализатора A
Получение, как описано в примере 5, но теперь использовали 0,55 мл TiCl4 вместо ТБТ.
Пример 7
Получение катализатора A
Получение, как описано в примере 3, но теперь количество агента переноса составляло 4 мл.
Пример 8
Получение катализатора A
Получение, как описано в примере 3, но теперь использовали 1,9 г моноэтилалюминийхлорида (МЭАХ) в качестве агента переноса.
Пример 9
Получение катализатора A
Получение, как описано в примере 3, но теперь с использованием 3,8 мл ТБТ.
Пример 10
Получение катализатора A
Получение, как описано в примере 3, причем вместо ТБТ использовали смесь 1,71 мл ТБТ и 2,36 г тетрахлорида циркония (ZrCl4). Эту смесь сначала готовили путем добавления 50 мл бензина к 50 мл толуола и последующего добавления 6,2 г ZrCl4 и 4,5 мл Ti(OBu)4 при непрерывном перемешивании.
Примеры 11-16
Полимеризация
Серии непрерывных (со)полимеризаций проводили в автоклаве с двойными стенками объемом 2 литра. С этой целью автоклав полностью заполняли бензином (это являлось смесью алифатических углеводородов с интервалом кипения 65-70oC). Бензин (5,50 кг/час), этилен (1270 г/час) и октен (810 г/час) непрерывно дозировали в этот реактор для получения этиленоктенового сополимера. Так подавалось определенное количество водорода. Температура реакции составляла 185oC. Давление поддерживалось на таком уровне, что автоклав оставался полным. Какое-то количество катализатора непрерывно дозированно подавалось в автоклав. К этому катализатору дозированно добавлялось какое-то количество триэтилалюминия (ТЭА) в качестве сокатализатора B. Сокатализатор B и катализатор перемешивали в течение 20 секунд перед подачей в автоклав. В примерах 11-16 полимеризации проводили с помощью катализаторов из примеров 1-6. Результаты полимеризации показаны в табл. 1. "Дозой кат." названа сумма масс металлов и галогенов на катализатора A в час. "Остаточный титан" и "остаточный хлор" относится к остаточным концентрациям титана и хлора, соответственно, в полиэтилене. Свойства продукта полиэтилена показаны в табл.1.
Примеры 17-23
Полимеризация
Полимеризации проводили, как описано в примерах 11-16. В примерах 17 и 18 использовали катализатор из примера 7. В примерах 19 и 20 использовали катализатор из примера 8. В примерах 21 и 22 использовали катализатор из примера 9. В примере 23 использовали катализатор из примера 10. Изопропилхлорид подавали непосредственно в автоклав в качестве дополнительного вещества, которое не реагирует спонтанно с магнийорганическим соединением, так что концентрация в автоклаве составляла 0,025 ммоль/л. ТЭА дозировали непосредственно в автоклав в качестве сокатализатора B. Результаты полимеризации показаны в табл. 2.
Примеры 24-26
Получение катализатора A и полимеризация
Катализатор A получали следующим образом. Изопропилхлорид (IpCl) использовали в качестве хлорида, который не реагирует спонтанно с магнийорганическим соединением. Его смешивали c BOMAG-A® в резервуаре для хранения. Применялось молярное отношение Cl:Mg, равное 2,2:1. В качестве агента переноса использовали 0,46 ммоль/час СЭАХ. TiCl4, растворенный в бензине, использовали в качестве соединения переходного металла. Смесь IpCl/ BOMAG-A® , СЭАХ и TiCl4 последовательно дозировали в подводящий трубопровод автоклава. В этом подводящем трубопроводе происходило смешивание BOMAG-A®, IpCl и СЭАХ в течение 50 секунд. После дозирования TiCl4 проходило примерно еще 20 секунд до того, как происходило введение в автоклав. ТЭА использовали в качестве сокатализатора В. Водород NI/час использовали в качестве регулятора длины цепи.
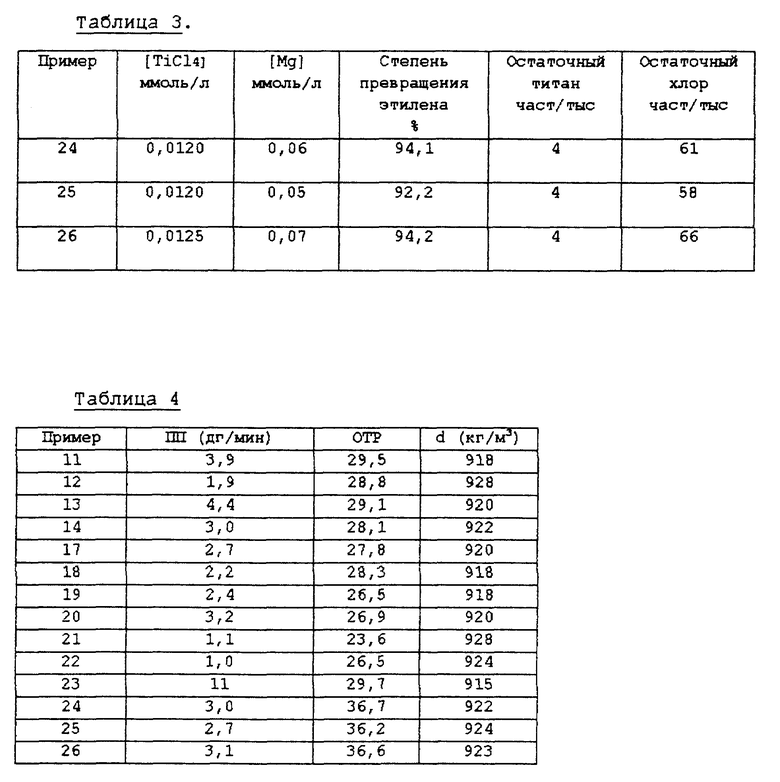
Другие условия полимеризации были такими же, какие описаны в примерах 11-16. Результаты полимеризации показаны в табл. 3.
Свойства продукта полиэтилена даны в табл. 4.
Эти примеры ясно показывают, что каталитическая система по этому изобретению очень активна, судя по полученным низким остаточным количествам и степени превращения этилена. Как видно из табл. 4, примеры 11-22 по сравнению с примерами 23-26, распределение молекулярного веса, выраженное в ОТР, можно прекрасно регулировать путем разных методов получения катализатора A.
Пример 27
Получение катализатора A
Весь процесс получения проводится с исключением воздуха и влаги и в инертной азотной атмосфере. Все реакции проводили при перемешивании с помощью стеклянной мешалки.
5 мл бензина вводили в стеклянную колбу. К этому в качестве агента переноса добавляли 4,5 мл СЭАХ (1 моль/л). Затем готовили смесь 25 мл бензина, 15 мл 15%-ного раствора бутилоктилмагния с 0,14% диэтилового эфира в гептане ( (BOMAG-D®, полученный от Witco) и 2,20 мл 2-хлорбутана. Это была прозрачная бесцветная жидкость. В течение двухчасового отрезка времени эту смесь затем добавляли по каплям при комнатной температуре при перемешивании к раствору СЭАХ в бензине. Образовывался осадок. После того, как весь BOMAG-D® добавлен, полученную смесь перемешивали при комнатной температуре в течение 3,5 часов. Затем к этой смеси по каплям в течение 0,5 часа добавляли 0,31 мл ТБТ в 25 мл бензина. После того, как добавлен раствор ТБТ, всю смесь перемешивали при комнатной температуре в течение двух часов.
Пример 28
Получение катализатора A
Весь процесс получения проводили с исключением воздуха и влаги и в инертной азотной атмосфере. Все реакции проводили при перемешивании с помощью стеклянной мешалки.
В стеклянную колбу вводили 10 мл бензина и 0,51 мл СЭАХ. Готовили смесь 20 мл бензина, 9 мл 20%-ного раствора бутилоктилмагнийэтоксида в гептане (BOMAG-O®, полученный от Witco) и 2,19 мл 2-хлорбутана. Затем в течение двухчасового отрезка времени эту смесь при комнатной температуре при перемешивании добавляли к раствору СЭАХ в бензине. Образовывался осадок. После того, как весь BOMAG-O® был добавлен, полученную смесь перемешивали при комнатной температуре в течение 3,5 часов. Затем к этой смеси в течение 0,5 часа по каплям добавляли 0,31 мл ТБТ в 20 мл бензина. После того, как добавлен раствор ТБТ, смесь перемешивали в течение 2 часов.
Пример 29
Получение катализатора A
Получение, как описано в примере 27, с 10 мл (20%) BOMAG-A® вместо 15 мл BOMAG-D® и 2,15 мл циклопентилхлорида вместо 2,20 мл 2-хлорбутана.
Пример 30
Получение катализатора A
Получение, как описано в примере 29, с 3,20 мл 3-хлорпентана вместо 2,15 мл циклопентилхлорида.
Пример 31
Получение катализатора A
Получение, как описано в примере 29, с 1,08 мл 2,2-дихлорпропана вместо 2,15 мл циклопентилхлорида.
Пример 32
Получение катализатора A
Получение, как описано в примере 29, со смесью 1,08 мл 1-хлорбутана и 1,10 мл 2-хлорбутана вместо 2,15 мл циклопентилхлорида.
Пример 33
Получение катализатора A
Получение, как описано в примере 32, с 2,11 мл 1-хлордекана вместо 1-хлорбутана.
Пример 34
Получение катализатора A
Получение, как описано в примере 28, с 10,1 мл BOMAG-A® вместо BOMAG-O® со смесью 0,55 мл 2-хлорбутана и 1,62 мл 1-хлорбутана вместо 2-хлорбутана. Смесь добавляли таким образом, что сначала в течение 0,5 часа добавляли 2-хлорбутан и после завершения добавления этого вещества добавляли 1-хлорбутан в течение 1,5 часов.
Пример 35
Получение катализатора A
Получение, как описано в примере 34, с 2,16 мл 1-хлорбутана вместо смеси 2-хлорбутана и 1-хлорбутана и 0,57 г моноэтилалюминийдихлорида (МЭАХ) вместо СЭАХ.
Пример 36
Получение катализатора A
Получение, как описано в примере 35, с 0,1 мл TiCl4 вместо ТБТ.
Пример 37
Получение катализатора A
Получение, как описано в примере 35, с 0,60 г трихлорида алюминия (AlCl3) вместо МЭАХ.
Пример 38
Получение катализатора A
Получение, как описано в примере 34, с 2,19 мл 2-хлорбутана вместо смеси 2-хлорбутана и 1-хлорбутана. В качестве агента переноса использовали 1,23 г дихлорида цинка (ZnCi2). После получения MgCl2 (перед добавлением соединения переходного металла) добавляли 0,37 мл триэтилалюминия (ТЭА). В качестве соединения переходного металла использовали 0,11 мл TiCl4.
Пример 39
Получение катализатора A
Получение, как описано в примере 38, с 15 мл BOMAG-D® вместо BOMAG-A®. ТЭА не добавляли.
Примеры 40-52
Полимеризация
Серии реакций (гомо)полимеризации с периодической загрузкой осуществляли в 1,3 л реакторе, который заполняли водородом до 1 бар. В реактор дозировали 500 мл пентаметилгептана (ПМГ) и подавали этилен до тех пор, пока общее давление в реакторе не достигало 20 бар. Реактор нагревали до желаемой температуры полимеризации, равной 185oC. Необходимое количество триэтилалюминия в качестве сокатализатора B и катализатор A смешивали при комнатной температуре, после чего эту смесь загружали в реактор для полимеризации. Давление в реакторе для полимеризации поддерживали на постоянном уровне с помощью подачи этилена. Через 10 минут реакцию останавливали, и полученный раствор полимера охлаждали, после чего полимер мог быть отделен от остального раствора. В примерах 40-52 реакции полимеризации проводили с помощью катализаторов из примеров 27-39. Результаты полимеризации показаны в табл. 5. [Ti] относится к концентрациям титана в реакторе. [ТЭА] относится к концентрации триэтилалюминия в реакторе.
| название | год | авторы | номер документа |
|---|---|---|---|
| ИНДЕНИЛЬНЫЕ СОЕДИНЕНИЯ, СПОСОБ ПОЛИМЕРИЗАЦИИ ОЛЕФИНА, ПОЛИОЛЕФИН | 1993 |
|
RU2128183C1 |
| Каталитическая система для сополимеризации этилена и 1-октена в растворе, способ ее получения и способ получения сополимера этилена и 1-октена | 1988 |
|
SU1706377A3 |
| КАТАЛИТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ПОЛИМЕРИЗАЦИИ ОЛЕФИНОВ | 1995 |
|
RU2135522C1 |
| КАТАЛИЗАТОР ПОЛИМЕРИЗАЦИИ ОЛЕФИНОВ И СПОСОБ ПОЛУЧЕНИЯ ПОЛИОЛЕФИНОВ | 1992 |
|
RU2088596C1 |
| КАТАЛИЗАТОР И СПОСОБ ПОЛИМЕРИЗАЦИИ ОЛЕФИНОВ | 1993 |
|
RU2116315C1 |
| СПОСОБ ПОЛУЧЕНИЯ НАНЕСЕННОГО КАТАЛИЗАТОРА ДЛЯ ПОЛИМЕРИЗАЦИИ ЭТИЛЕНА И СОПОЛИМЕРИЗАЦИИ ЭТИЛЕНА С АЛЬФА-ОЛЕФИНАМИ | 1994 |
|
RU2064836C1 |
| СПОСОБ ПОЛУЧЕНИЯ КАТАЛИЗАТОРА ДЛЯ ПОЛИМЕРИЗАЦИИ ЭТИЛЕНА | 1982 |
|
SU1053352A1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ КАТАЛИЗАТОРА И ПРОЦЕСС ПОЛИМЕРИЗАЦИИ ЭТИЛЕНА И СОПОЛИМЕРИЗАЦИИ ЭТИЛЕНА С АЛЬФА-ОЛЕФИНАМИ С ИСПОЛЬЗОВАНИЕМ ЭТОГО КАТАЛИЗАТОРА | 2004 |
|
RU2257263C1 |
| Катализатор для полимеризации олефинов,каталитическая система для полимеризации олефинов, способ получения катализатора для полимеризации олефинов и способ полимеризации этилена или сополимеризации этилена с пропиленом | 1979 |
|
SU1055320A3 |
| КАТАЛИЗАТОР ПОЛИМЕРИЗАЦИИ ПРОПИЛЕНА, КАТАЛИТИЧЕСКАЯ СИСТЕМА И СПОСОБ ПОЛУЧЕНИЯ ПОЛИПРОПИЛЕНА | 1991 |
|
RU2074864C1 |



Группа изобретений относится к каталитической системе для гомополимеризации этилена и сополимеризации этилена с одним или более α-олефинов или неконьюгированных диенов, а также к получению каталитической системы и к сополимеризации этилена с помощью каталитической системы. Каталитическая система состоит из катализатора А, сокатализатора В и агента переноса, причем катализатор А включает одно или более магнийорганических соединений, соединений переходных металлов и органический хлорид, который не реагирует спонтанно с магнийорганическими соединениями. При осуществлении способа получения каталитической системы магнийорганическое соединение смешивают с органическим хлоридом, и полученную смесь добавляют к раствору агента переноса. При проведении полимеризации этилена используют вышеуказанную каталитическую систему в газовой фазе, суспензии, растворе и для полимеризации в массе. Помимо каталитической системы возможно добавление в реактор органических хлоридов, не реагирующих спонтанно с магнийорганическими соединениями. Достигается облегчение и упрощение контролирования реакции при получении катализатора, повышение активности катализатора при высоких температурах и выхода получаемого полимера. 3 с. и 21 з.п. ф-лы, 5 табл.
| NL 7605544 A, 30.11.76 | |||
| Вагон, преимущественно типа думпкара, с откидывающимся продольным бортом, опережающим поворот кузова при разгрузке | 1959 |
|
SU126515A1 |
| 0 |
|
SU403194A1 | |
| Способ получения (со) полимеров этилена | 1976 |
|
SU665687A1 |
| Катализатор(со) полимеризации этилена | 1975 |
|
SU727149A3 |
| СПОСОБ ПОЛУЧЕНИЯ ОКСИМКАРБАМАТОВ | 0 |
|
SU280353A1 |
| Устройство для выборки орудий лова | 1975 |
|
SU514594A1 |
| Способ приготовления сернистого красителя защитного цвета | 1921 |
|
SU84A1 |
| US 4496660 A, 29.01.85 | |||
| US 4387200 A, 07.06.83 | |||
| СПОСОБ ПОЛУЧЕНИЯ ВАКУУМНОПЛОТНОГО СОЕДИНЕНИЯ МЕТАЛЛ —ПОЛУПРОВОДНИК | 0 |
|
SU351266A1 |
| Устройство для вращательного колонкового бурения | 1929 |
|
SU43582A1 |
| ГИДРОМАШИНА ВОЛНОВОГО ТИПА | 0 |
|
SU280352A1 |
Авторы
Даты
1999-12-10—Публикация
1995-06-26—Подача