ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к применению ингибиторов PRMT5 (белок аргинин N-метилтрансфераза 5), таких как и включая (1S,2S,3S,5R)-3-((6-(дифторметил)-5-фтор-1,2,3,4-тетрагидроизохинолин-8-ил)окси)-5-(4-метил-7H-пирроло[2,3-d]пиримидин-7-ил)циклопентан-1,2-диол, имеющего структуру:
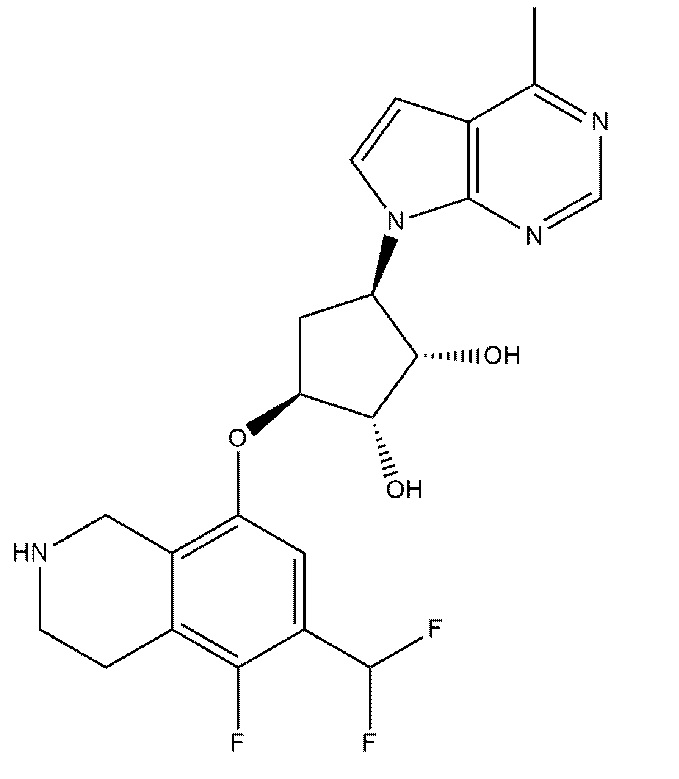 ,
,
или его фармацевтически приемлемую соль, для лечения псориаза, системной красной волчанки (называемой также "SLE" или "волчанкой"), ревматоидного артрита (RA), псориатического артрита и других аутоиммунных состояний или нарушений.
УРОВЕНЬ ТЕХНИКИ
Псориаз (иногда называемый "бляшечным псориазом") является хроническим заболеванием кожи, которым страдают приблизительно 2-4 процента населения мира. В США этим заболеванием поражены свыше семи миллионов человек. Несмотря на то что патогенез псориаза еще полностью не выяснен, тем не менее существуют важные доказательства, указывающие на то, что эпидермальные изменения возникают в качестве вторичного иммунного ответа на клеточные иммунные инфильтраты в коже. Псориаз характеризуется дискретными участками воспаления кожи с покраснением, утолщением, интенсивным шелушением и, в некоторых случаях, зудом. Заболевание оказывает значительное негативное влияние на качество жизни страдающих этим заболеванием людей, как физическое, так и психологическое. На сегодняшний день не существует лекарственного средства для излечения псориаза, и лечение направлено на уменьшение тяжести и распространения псориатических бляшек и связанных с ними симптомов. Основным показателем успеха лечения, используемым Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США при оценке лекарственных препаратов для лечения псориаза, является значительное общее облегчение тяжести псориаза на основе проводимой исследователями общей оценки.
Лечение псориаза, в зависимости от тяжести и ответных реакций на терапию, включает местную или системную медикаментозную терапию, фототерапию и различные вспомогательные методы лечения, такие как, применение увлажняющих средств и салициловой кислоты. Системное терапевтическое лечение более поздних стадий псориаза включает применение метотрексата, циклоспорина и других синтетических или биологических препаратов, таких как инфликсимаб, этанерцепт и устекинумаб. Американская академия дерматологии (AAD) уже на протяжении длительного времени занимается разработкой серии клинических рекомендаций по лечению псориаза и псориатического артрита (https://www.aad.org/member/clinical-quality/guidelines). Но несмотря на эти медицинские достижения, в медицине все еще существует неудовлетворенная потребность в разработке более безопасных, эффективных и удобных лекарственных препаратов для лечения псориаза. Другие хронические аутоиммунные состояния, такие как системная красная волчанка, ревматоидный артрит и псориатический артрит, также трудно поддаются эффективному лечению и/или полному излечению.
Не приводя в качестве доказательства описанный ниже механизм действия, тем не менее, можно предположить, что PRMT5 и его партнер по связыванию MEP50 образуют метилосомный комплекс, который использует S-аденозилметионин для переноса метильных групп для аргинина, катализируя как моно-, так и симметричное диметилирование на остатках субстрата. PRMT5 метилирует многие белковые субстраты, принимающие участие в транскрипции, в системе клеточных сигналов, в трансляции мРНК, в повреждении ДНК, в трафике рецептора, в стабильности белков и в сплайсинге пре-мРНК. Наиболее хорошо изученные из субстратов PRMT5 являются сплайсомные белки сборки, которые регулируют сплайсинг пре-мРНК. Мутации сайтов сплайсинга, мутации фактора сплайсинга и изменения активности сплайсинга связывают с развитием и прогрессированием рака. PRMT5 симметрично диметилирует белки, которые регулируют сплайсинг пре-мРНК, включая сплайсомные белки, SmD1, SmD3 и SmB/B. Это метилирование повышает аффинность Sm белков к домену tudor белка SMN1, что облегчает сборку комплексов малого ядерного рибонуклеопротеина (snRNP) для надлежащего распознавания сайта сплайсинга и рекрутмента дополнительных факторов сплайсинга. Результаты исследования условного нокаута PRMT5 в нервных стволовых клетках/клетках-предшественниках (NPC) мышей позволяет сделать вывод о том, что функция PRMT5 необходима для правильного выбора сайта сплайсинга. Генетическое ингибирование PRMT5 приводит к повышенному удержанию интронов и пропуску экзонов в пре-мРНК, что приводит к нонсенс-опосредованному распаду мРНК или к альтернативному сплайсингу мРНК. Эти альтерации сплайсинга могут снижать экспрессию белков или генерировать альтернативные "неправильно сплайсированные" изоформы белка с непредсказуемой функцией по регуляции клеточного цикла, репликации и репарации ДНК, метаболизма и каскада иммунных реакций.
Альтернативный сплайсинг и экспрессию факторов сплайсинга также ассоциируют с аутоиммунными заболеваниями, включая: псориаз (Li J, Yu P. Genome-wide transcriptome analysis identifies alternative splicing regulatory network and key splicing factors in mouse and human psoriasis. Sci Rep. 2018;8(1):4124. Published 2018 Mar 7), системную красную волчанку (Odhams CA, Cortini A, Chen L, et al. Mapping eQTLs with RNA-seq reveals novel susceptibility genes, non-coding RNAs and alternative-splicing events in systemic lupus erythematosus. Hum Mol Genet. 2017;26(5):1003-1017) и ревматоидный артрит (Shchetynsky K, Protsyuk D, Ronninger M, Diaz-Gallo LM, Klareskog L, Padyukov L. Gene-gene interaction and RNA splicing profiles of MAP2K4 gene in rheumatoid arthritis. Clin Immunol. 2015;158(1):19-28). Данные по секвенированию РНК при сравнении мышей с нокаутом Tnip и людей, страдающих псориазом, выявили 18 консервативных кассетных экзонов, которые могут быть связаны с заболеванием (Li et al., смотрите выше), в следующих генах: ABI1, ARHGAP12, ATP5C1, CTTN, DMN1L, EXOC1, FBLN2, FNBP1, GOLGA2, GOLGA4, MYH11, MYL6, MYO1B, PAM, SEC31A, SLK, SPAG9 и ZMYND11Additionally, были идентифицированы двенадцать факторов сплайсинга (CELF1, CELF2, DDX5, MBNL1,MBNL2, NOVA1, PRMT5, PTBP1, RBFOX2, SF3A1, SRRM4 и U2AF1), в том числе PRMT5, который может способствовать возникновению псориаза в результате альтернативного регулирования сплайсинга генов, важного при протекания каскада реакций, связанных с псориазом. Внутренние данные по секвенированию РНК позволили идентифицировать несколько из этих экзонов (ABI1, CTTN, EXOC1, GOLGA4, MYL6, PAM и SEC31A) и факторов сплайсинга (MBNL1, PTBP1 и U2AF1) в качестве мишеней для альтернативного сплайсинга при воздействии ингибиторов PRMT5.
В случае системной красной волчанки, 25% пациентов имеют ответ аутоиммунного антитела к антигену Смита (Sm), который включает сплайсомные белки SmB, SmD1 и SmD3 (Kalinina O, Louzoun Y, Wang Y, Utset T, Weigert M. Origins and specificity of auto-antibodies in Sm+ SLE patients. J Autoimmun. 2018; 90:94-104). PRMT5 симметрично диметилирует аргинины на всех трех из этих белков, и такое метилирование повышает их антигенность. Большинство из антител против Sm направлены на эти эпитопы. Удаление остатков метиларгинина из белков Sm у пациентов, страдающих системной красной волчанкой, с помощью ингибитора PRMT5, может снижать ответ аутоиммунного антитела путем редукции триггерного антигена.
PRMT5 также принимает определенное участие в сигнальном пути NF-kB, который является важным путем, вовлеченным в хроническое воспаление. Субъединица p65 фактора транскрипции NF-kB непосредственно метилируется на различных остатках аргинина (R30, R34 и R174), что воздействует на рекрутмент NF-kB до 78% из его промоторов гена-мишени, включая TRAF1, IL1A, CXCL10 и CXCL11 (Harris DP, Bandyopadhyay S, Maxwell TJ, Willard B, DiCorleto PE. Tumor necrosis factor (TNF)-α induction of CXCL10 in endothelial cells requires protein arginine methyltransferase 5 (PRMT5)-mediated nuclear factor (NF)-κB p65 methylation. J Biol Chem. 2014;289(22):15328-15339; Harris DP, Chandrasekharan UM, Bandyopadhyay S, Willard B, DiCorleto PE. PRMT5-Mediated Methylation of NF-κB p65 at Arg174 Is Required for Endothelial CXCL11 Gene Induction in Response to TNF-α and IFN-γ Costimulation. PLoS One. 2016;11(2) published 2016 Feb 22; and Wei H, Wang B, Miyagi M, et al. PRMT5 dimethylates R30 of the p65 subunit to activate NF-κB. Proc Natl Acad Sci USA. 2013;110(33):13516-13521). Ингибиторы PRMT5 можно было бы применять для блокирования цитокина, индуцированного экспрессией NF-kB гена-мишени, что, по-видимому, приводило к уменьшению воспаления.
В патентном документе U.S. Patent No. 10220037 раскрыты различные соединения и композиции, относительно которых известно, что они ингибируют PRMT5 и оказывают лечебное действие при раке. Среди этих соединений, описанных в патентном документе U.S. Patent No. 10220037, находится (1S,2S,3S,5R)-3-((6-(дифторметил)-5-фтор-1,2,3,4-тетрагидроизохинолин-8-ил)окси)-5-(4-метил-7H-пирроло-[2,3-d]пиримидин-7-ил)циклопентан-1,2-диол или его фармацевтически приемлемая соль. О применении этих соединений помимо онкологии не было известно.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В настоящем изобретении раскрыты способы лечения субъекта (или пациента), страдающего от аутоиммунного состояния или нарушения, где способы включают введение субъекту, нуждающемуся в этом, терапевтически эффективного количества ингибитора PRMT5. Ингибитор PRMT5 может представлять собой любой ингибитор PRMT5 или комбинацию одного или более ингибиторов PRMT5. Например, один или более ингибиторов PRMT5, выбранных из известных ингибиторов, могут применяться для лечения аутоиммунных нарушений, в том числе (1S,2S,3S,5R)-3-((6-(дифторметил)-5-фтор-1,2,3,4-тетрагидро-изохинолин-8-ил)окси)-5-(4-метил-7H-пирроло[2,3-d]пиримидин-7-ил)циклопентан-1,2-диол или его фармацевтически приемлемая соль.
В некоторых вариантах осуществления, аутоиммунное нарушение выбирают из группы, состоящей из псориаза, атопического дерматита, очаговой алопеции, анкилозирующего спондилита, астмы, сахарного диабета I типа, множественного склероза, целиакии, склеродермии, гнойного гидраденита, витилиго, дерматомиозита, системной красной волчанки, ревматоидного артрита, псориатического артрита и воспалительного заболевания кишечника.
В некоторых вариантах осуществления, субъекту вводят терапевтически эффективное количество ингибитора PRMT5 энтерально (например, перорально или ректально), парентерально (например, внутривенно или внутрисуставно), или местно. В некоторых вариантах осуществления, субъекту вводят терапевтически эффективное количество от приблизительно 0,5 мг до приблизительно 120 мг. В некоторых вариантах осуществления, терапевтически эффективное количество составляет приблизительно 0,5 мг, 1 мг, 2 мг, 4 мг, 6 мг, 8 мг, 10 мг, 16 мг, 32 мг, 60 мг или 120 мг. В некоторых вариантах осуществления, терапевтически эффективное количество вводят один раз в сутки (QD) или два раза в сутки (BID). В некоторых вариантах осуществления, терапевтически эффективное количество вводят в течение от 1 до 28 дней, 1-6 недель, 1-4 месяца, или 1-6 месяцев.
Это изобретение относится к ингибитору PRMT5, в частности, к (1S,2S,3S,5R)-3-((6-(дифторметил)-5-фтор-1,2,3,4-тетрагидро-изо-хинолин-8-ил)окси)-5-(4-метил-7H-пирроло[2,3-d]пиримидин-7-ил)-циклопентан-1,2-диолу, для применения при лечении аутоиммунного состояния или нарушения; или для применения при производстве лекарственного препарата, используемого при лечении аутоиммунного состояния или нарушения.
ПОДРОБНОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
На фигуре 1A изображена кожа пациента с псориазом, передняя сторона торса, после проведения лечения путем введения два раза в сутки 1 мг (1S,2S,3S,5R)-3-((6-(дифторметил)-5-фтор-1,2,3,4-тетрагидроизохинолин-8-ил)окси)-5-(4-метил-7H-пирроло[2,3-d]-пиримидин-7-ил)циклопентан-1,2-диола в течение двух недель. Симптомы псориаза умеренно выражены.
На фигуре 1B изображена кожа пациента с псориазом, передняя сторона торса, после проведения лечения путем введения два раза в сутки 1 мг (1S,2S,3S,5R)-3-((6-(дифторметил)-5-фтор-1,2,3,4-тетрагидроизохинолин-8-ил)окси)-5-(4-метил-7H-пирроло[2,3-d]-пиримидин-7-ил)циклопентан-1,2-диола в течение шести недель. Симптомы псориаза слабо выражены.
На фигуре 2A изображена кожа пациента с псориазом, задняя сторона торса, после проведения лечения путем введения два раза в сутки 1 мг (1S,2S,3S,5R)-3-((6-(дифторметил)-5-фтор-1,2,3,4-тетрагидроизохинолин-8-ил)окси)-5-(4-метил-7H-пирроло[2,3-d]-пиримидин-7-ил)циклопентан-1,2-диола в течение двух недель. Симптомы псориаза умеренно выражены.
На фигуре 2B изображена кожа пациента с псориазом, задняя сторона торса, после проведения лечения путем введения два раза в сутки 1 мг (1S,2S,3S,5R)-3-((6-(дифторметил)-5-фтор-1,2,3,4-тетрагидроизохинолин-8-ил)окси)-5-(4-метил-7H-пирроло[2,3-d]-пиримидин-7-ил)циклопентан-1,2-диола в течение шести недель. Симптомы псориаза слабо выражены.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Приведенное далее подробное описание предпочтительных вариантов осуществления изобретения и включенные в изобретение примеры позволяют легче понять настоящее изобретение. Следует иметь в виду, что используемая в изобретении терминология предназначена только для описания конкретных вариантов осуществления и никоим образом не ограничивает изобретение. Кроме того, следует иметь в виду, что, если в изобретении терминология специально не определена, то терминология, используемая в изобретении, должна иметь свое общепринятое для соответствующей области техники значение.
Соединения, применяемые в настоящем изобретении, включают ингибитор PRMT5 (1S,2S,3S,5R)-3-((6-(дифторметил)-5-фтор-1,2,3,4-тетрагидроизохинолин-8-ил)окси)-5-(4-метил-7H-пирроло[2,3-d]-пиримидин-7-ил)циклопентан-1,2-диол и его фармацевтически приемлемые соли.
Другие ингибирующие PRMT5 соединения, применяемые в настоящем изобретении, включают, но этим не ограничивая, GSK3326595 (GlaxoSmithKline; CAS No.: 1616392-22-3), JNJ-64619178 (Johnson & Johnson; CAS No.: 2086772-26-9), CTx-034 (Cancer Therapeutics), PRMT5-04 (Auigene Discovery Technologies), EPZ015666 (Epizyme/GlaxoSmithKline), LLY283 и LLY-284 (Eli Lilly; смотрите, например, Bonday et al., LLY-283, a Potent and Selective Inhibitor of Arginine Methyltransferase 5, PRMT5, with Antitumor Activity. ACS Med Chem Lett. 2018; 9(7): 612-617), PRT543 and PRT811 (Prelude Therapeutics), и другие соединения.
Согласно первому аспекту изобретения, предлагается способ лечения аутоиммунного состояния или нарушения у субъекта, нуждающегося в этом, включающий введение субъекту терапевтически эффективного количества ингибитора PRMT5.
Ниже описываются варианты осуществления (E) этого первого аспекта изобретения, где, для удобства, E1 является идентичным ему.
E1. Способ лечения аутоиммунного нарушения у субъекта, нуждающегося в этом, включающий введение субъекту терапевтически эффективного количества ингибитора PRMT5.
E2. Способ по варианту осуществления E1, где ингибитор PRMT5 выбирают из группы, состоящей из (1S,2S,3S,5R)-3-((6-(дифторметил)-5-фтор-1,2,3,4-тетрагидроизохинолин-8-ил)окси)-5-(4-метил-7H-пирроло[2,3-d]пиримидин-7-ил)циклопентан-1,2-диола, GSK3326595, JNJ-64619178, CTx-034, PRMT5-04, EPZ015666, LLY283, LLY-284, PRT543, PRT811; и их фармацевтически приемлемых солей.
E3. Способ по любому одному из вариантов осуществления E1 - E2, где ингибитор PRMT5 представляет сбой 1S,2S,3S,5R)-3-((6-(дифторметил)-5-фтор-1,2,3,4-тетрагидроизохинолин-8-ил)окси)-5-(4-метил-7H-пирроло[2,3-d]пиримидин-7-ил)циклопентан-1,2-диол или его фармацевтически приемлемую соль.
E4. Способ по любому одному из вариантов осуществления E1 - E3, где аутоиммунное нарушение выбирают из группы, состоящей из ревматоидного артрита, ревматоидного артрита с системными проявлениями, ревматоидного полиартрита, энтеропатического артрита, спондилоартропатии, энтеропатического спондилита, реактивного артрита, аксиального спондилоартрита, анкилозирующего спондилита, псориатического артрита, неаксиального спондилоартрита, остеоартрита, подагрического артрита, ювенильного артрита, ювенильного ревматоидного артрита, ювенильного ревматоидного артрита с системными проявлениями, периартикулярного ювенильного ревматоидного артрита, болезни Стилла, ювенильного синдрома Рейтера, ювенильного анкилозирующего спондилита, ювенильного энтеропатического артрита, ювенильного идиопатического артрита, ювенильного псориатического артрита, тиреоидита Хашимото, аутоиммунной гемолитической анемии, аутоиммунного атрофического гастрита и пернициозной анемии, аутоиммунного энцефаломиелита, аутоиммунного орхита, васкулита, болезни Гудпасчера, аутоиммунной тромбоцитопении, симпатической офтальмии, миастении гравис, синдрома Гийена-Барре, болезни Грейвcа, первичного биллиарного цирроза, аутоиммунного гепатита, первичного склерозирующего холангита, хронического агрессивного гепатита, неалкогольного жирового гепатоза, неалкогольного стеатогепатита, цирроза, мембранозной гломерулопатии, фокально-сегментарного гломерулосклероза, синдрома Альпорта, IgA-нефропатии, волчанки, системной волчанки, системной красной волчанки (SLE), ювенильной системной красной волчанки (SLE), волчаночного нефрита, идиопатического панкреатита, синдрома Шегрена, миозита и полимиозита, дерматомиозита, интерферонопатий I типа, синдрома Айкарди-Гутьерес, системного склероза, артериита, нодозного полиартериита, множественного склероза, возвратно- ремиттирующего множественного склероза, первичного прогрессирующего множественного склероза, вторичного прогрессирующего множественного склероза, буллезного пемфигоида, синдрома Когана, гранулематоза Вегенера, аутоиммунной алопеции, васкулита, нефрита, болезни Бехчета, ревматической полимиалгии, гигантоклеточного артериита, воспаления хряща, разрушения кости, тиреоидита, сахарного диабета первого типа, целиакий, проктита, эозинофильного гастроэнтерита, эозинофильного эзофагита, мастоцитоза, воспалительного заболевания кишечника, экземы, хронической экземы на руках, дисгидротической экземы, хронического зуда, атопического дерматита, контактного аллергического дерматита, аллергического дерматита, периорального дерматита, застойного дерматита, ирритантного дерматита, монетовидного дерматита, профессионального дерматита, себорейного дерматита, ксеротического дерматита, дерматита век глаза, пеленочного дерматита, дерматита кистей рук, дерматомиозита, нейродермита, красного плоского лишая, склероатрофического лишая, витилиго, очаговой алопеции, прурита, псориаза, бляшечного псориаза, каплевидного псориаза, инверсного псориаза, пустулезного псориаза, псориаза ногтей, ладонно-подошвенного псориаза, псориаза на лице или эритродермического псориаза, розовых угрей, склеродермии, обыкновенной пузырчатки, покраснения кожи, кожной волчанки, келоидного рубца, рубца от солнечного ожога, гипертрофического рубца, идиопатической тромбоцитопенической тромботической пурпуры, ихтиоза, эпидермальной гиперплазии, угрей, буллезного эпидермоза, опрелости, волосяного лишая, крапивницы, контагиозного моллюска, синдрома Незертона, синдрома Фогта-Коянаги-Харада, синдрома Свита, себорейной экземы, обыкновенной пузырчатки, вульвовагинита, невуса/невусов Сеттона, поствоспалительной гипопигментации, сенильной лейкодермы, лейкодермы, вызванной воздействием химического/лекарственного вещества, кожной красной волчанки, дискоидной волчанки, ладонно-подошвенного пустулеза, пемфигоида и гнойного гидраденита.
E5. Способ по любому одному из вариантов осуществления E1 - E4, где аутоиммунное нарушение выбирают из группы, состоящей из псориаза, атопического дерматита, очаговой алопеции, анкилозирующего спондилита, астмы, сахарного диабета I типа, множественного склероза, целиакии, склеродермии, гнойного гидраденита, витилиго, дерматомиозита, системной красной волчанки, ревматоидного артрита, псориатического артрита и воспалительного заболевания кишечника.
E6. Способ по любому одному из вариантов осуществления E1 - E5, где аутоиммунное нарушение представляет собой псориаз.
E7. Способ по любому одному из вариантов осуществления E1 - E5, где аутоиммунное нарушение представляет собой атопический дерматит.
E8. Способ по любому одному из вариантов осуществления E1 - E5, где аутоиммунное нарушение представляет собой очаговую алопецию.
E9. Способ по любому одному из вариантов осуществления E1 - E5, где аутоиммунное нарушение представляет собой анкилозирующий спондилит.
E10. Способ по любому одному из вариантов осуществления E1 - E5, где аутоиммунное нарушение представляет собой астму.
E11. Способ по любому одному из вариантов осуществления E1 - E5, где аутоиммунное нарушение представляет собой сахарный диабет I типа.
E12. Способ по любому одному из вариантов осуществления E1 - E5, где аутоиммунное нарушение представляет собой множественный склероз.
E13. Способ по любому одному из вариантов осуществления E1 - E5, где аутоиммунное нарушение представляет собой целиакию.
E14. Способ по любому одному из вариантов осуществления E1 - E5, где аутоиммунное нарушение представляет собой склеродермию.
E15. Способ по любому одному из вариантов осуществления E1 - E5, где аутоиммунное нарушение представляет собой гнойный гидраденит.
E16. Способ по любому одному из вариантов осуществления E1 - E5, где аутоиммунное нарушение представляет собой витилиго.
E17. Способ по любому одному из вариантов осуществления E1 - E5, где аутоиммунное нарушение представляет собой дерматомиозит.
E18. Способ по любому одному из вариантов осуществления E1 - E5, где аутоиммунное нарушение представляет собой системную красную волчанку.
E19. Способ по любому одному из вариантов осуществления E1 - E5, где аутоиммунное нарушение представляет собой ревматоидный артрит.
E20. Способ по любому одному из вариантов осуществления E1 - E5, где аутоиммунное нарушение представляет собой псориатический артрит.
E21. Способ по любому одному из вариантов осуществления E1 - E5, где аутоиммунное нарушение представляет собой воспалительное заболевание кишечника.
E22. Способ по варианту осуществления E21, где воспалительное заболевание кишечника представляет собой болезнь Крона.
E23. Способ по варианту осуществления E21, где воспалительное заболевание кишечника представляет собой язвенный колит.
E24. Способ по любому одному из вариантов осуществления E1 - E23, где терапевтически эффективное количество составляет от приблизительно 0,5 мг до приблизительно 120 мг.
E25. Способ по любому одному из вариантов осуществления E1 - E24, где терапевтически эффективное количество выбирают из группы, состоящей из приблизительно 0,5 мг, 1 мг, 2 мг, 4 мг, 6 мг, 8 мг, 10 мг, 16 мг, 32 мг, 60 мг, 80 мг и 120 мг.
E26. Способ по любому одному из вариантов осуществления E1 - E25, где терапевтически эффективное количество составляет приблизительно 1 мг.
E27. Способ по любому одному из вариантов осуществления E1 - E25, где терапевтически эффективное количество составляет приблизительно 120 мг.
E28. Способ по любому одному из вариантов осуществления E1 - E25, где терапевтически эффективное количество составляет приблизительно 60 мг.
E29. Способ по любому одному из вариантов осуществления E1 - E25, где терапевтически эффективное количество составляет приблизительно 32 мг.
E30. Способ по любому одному из вариантов осуществления E1 - E25, где терапевтически эффективное количество составляет приблизительно 16 мг.
E31. Способ по любому одному из вариантов осуществления E1 - E25, где терапевтически эффективное количество составляет приблизительно 10 мг.
E32. Способ по любому одному из вариантов осуществления E1 - E25, где терапевтически эффективное количество составляет приблизительно 8 мг.
E33. Способ по любому одному из вариантов осуществления E1 - E25, где терапевтически эффективное количество составляет приблизительно 6 мг.
E34. Способ по любому одному из вариантов осуществления E1 - E25, где терапевтически эффективное количество составляет приблизительно 4 мг.
E35. Способ по любому одному из вариантов осуществления E1 - E25, где терапевтически эффективное количество составляет приблизительно 2 мг.
E36. Способ по любому одному из вариантов осуществления E1 - E25, где терапевтически эффективное количество составляет приблизительно 0,5 мг.
E37. Способ по любому одному из вариантов осуществления E1 - E36, где терапевтически эффективное количество вводят один раз в сутки (QD).
E38. Способ по любому одному из вариантов осуществления E1 - E36, где терапевтически эффективное количество вводят два раза в сутки (QD).
E39. Способ по любому одному из вариантов осуществления E1 - E38, где терапевтически эффективное количество вводят в течение от 1 до 28 дней.
E40. Способ по любому одному из вариантов осуществления E1 - E38, где терапевтически эффективное количество вводят в течение от 1 до 6 недель.
E41. Способ по любому одному из вариантов осуществления E1 - E38, где терапевтически эффективное количество вводят в течение от 1 до 6 месяцев.
E42. Способ по любому одному из вариантов осуществления E1 - E38, где терапевтически эффективное количество вводят в течение от 1 до 4 месяцев.
E43. Способ по любому одному из вариантов осуществления E1 - E42, где ингибитор PRMT5 вводят энтерально, парентерально или местно.
E44. Способ по варианту осуществления Е43, где указанное энтеральное введение проводят перорально или ректально.
E45. Способ по варианту осуществления Е44, где указанное пероральное введение проводят в форме таблетке, капсулы или в жидкой лекарственной форме.
E46. Способ по варианту осуществления Е43, где указанное парентеральное введение проводят внутривенно или внутрисуставно.
E47. Способ по варианту осуществления Е43, где указанное местное введение проводят в форме раствора, крема, мази, геля, лосьона, суспензии или эмульсии.
E48. Способ по любому одному из вариантов осуществления E1 - E47, дополнительно включающий введение дополнительного терапевтически эффективного средства.
В некоторых вариантах осуществления, в случае перорального введения, (1S,2S,3S,5R)-3-((6-(дифторметил)-5-фтор-1,2,3,4-тетрагидроизохинолин-8-ил)окси)-5-(4-метил-7H-пирроло[2,3-d]-пиримидин-7-ил)циклопентан-1,2-диол или его фармацевтически приемлемая соль могут быть введены в форме таблетки, капсулы или в жидкой лекарственной форме (суспензии, сиропа или раствора).
В некоторых вариантах осуществления, в случае парентерального введения, (1S,2S,3S,5R)-3-((6-(дифторметил)-5-фтор-1,2,3,4-тетрагидроизохинолин-8-ил)окси)-5-(4-метил-7H-пирроло[2,3-d]-пиримидин-7-ил)циклопентан-1,2-диол или его фармацевтически приемлемая соль могут быть введены внутривенно (IV). Внутривенная инфузия может быть скорректирована так, чтобы при различных скоростях потока достигалась доставка терапевтически эффективного количества.
В некоторых вариантах осуществления, в случае парентерального введения, (1S,2S,3S,5R)-3-((6-(дифторметил)-5-фтор-1,2,3,4-тетрагидроизохинолин-8-ил)окси)-5-(4-метил-7H-пирроло[2,3-d]-пиримидин-7-ил)циклопентан-1,2-диол или его фармацевтически приемлемая соль могут быть введены в форме внутрисуставной инъекции.
В случае местного применения, (1S,2S,3S,5R)-3-((6-(дифторметил)-5-фтор-1,2,3,4-тетрагидроизохинолин-8-ил)окси)-5-(4-метил-7H-пирроло[2,3-d]пиримидин-7-ил)циклопентан-1,2-диол или его фармацевтически приемлемая соль могут быть нанесены во многих различных лекарственных формах, хорошо известных специалистам в данной области. Эти формы включают раствор, крем, мазь, гель, лосьон, суспензию или эмульсию, и другие подобные формы.
В случае ректального введения, (1S,2S,3S,5R)-3-((6-(дифторметил)-5-фтор-1,2,3,4-тетрагидроизохинолин-8-ил)окси)-5-(4-метил-7H-пирроло[2,3-d]пиримидин-7-ил)циклопентан-1,2-диол или его фармацевтически приемлемая соль могут быть введены в форме суппозитория, которая осуществляет доставку терапевтически эффективного количества описанного выше соединения.
Независимо от лекарственной формы, терапевтически эффективное количество (1S,2S,3S,5R)-3-((6-(дифторметил)-5-фтор-1,2,3,4-тетрагидроизохинолин-8-ил)окси)-5-(4-метил-7H-пирроло[2,3-d]-пиримидин-7-ил)циклопентан-1,2-диола составляет от приблизительно 0,5 мг до приблизительно 120 мг или более, вводимое один раз в сутки, более конкретно, 0,5 мг, 0,6 мг, 0,7 мг, 0,8 мг, 0,9 мг, 1 мг, 2 мг, 3 мг, 4 мг, 5 мг, 6 мг, 7 мг, 8 мг, 9 мг, 10 мг, 11 мг, 12 мг, 13 мг, 14 мг, 15 мг, 16 мг, 17 мг, 18 мг, 19 мг, 20 мг, 21 мг, 22 мг, 23 мг, 24 мг, 25 мг, 26 мг, 27 мг, 28 мг, 29 мг, 30 мг, 31 мг, 32 мг, 33 мг, 34 мг, 35 мг, 36 мг, 37 мг, 38 мг, 39 мг, 40 мг, 41 мг, 42 мг, 43 мг, 44 мг, 45 мг, 46 мг, 47 мг, 48 мг, 49 мг, 50 мг, 51 мг, 52 мг, 53 мг, 54 мг, 55 мг, 56 мг, 57 мг, 58 мг, 59 мг, 60 мг, 61 мг, 62 мг, 63 мг, 64 мг, 65 мг, 66 мг, 67 мг, 68 мг, 69 мг, 70 мг, 75 мг, 80 мг, 90 мг, 100 мг, 105 мг, 110 мг, 115 мг или 120 мг, или другие дозы, один раз в сутки.
В некоторых вариантах осуществления, терапевтически эффективное количество (1S,2S,3S,5R)-3-((6-(дифторметил)-5-фтор-1,2,3,4-тетрагидроизохинолин-8-ил)окси)-5-(4-метил-7H-пирроло-[2,3-d]пиримидин-7-ил)циклопентан-1,2-диола представляет собой дозу от приблизительно 0,05 мкг/кг до приблизительно 1000 мг/кг, от приблизительно 2 мг/кг до приблизительно 900 мг/кг, от приблизительно 3 мг/кг до приблизительно 800 мг/кг, от приблизительно 4 мг/кг до приблизительно 700 мг/кг, от приблизительно 5 мг/кг до приблизительно 600 мг/кг, от приблизительно 6 мг/кг до приблизительно 550 мг/кг, от приблизительно 7 мг/кг до приблизительно 500 мг/кг, от приблизительно 8 мг/кг до приблизительно 450 мг/кг, от приблизительно 9 мг/кг до приблизительно 400 мг/кг, от приблизительно 5 мг/кг до приблизительно 200 мг/кг, от приблизительно 2 мг/кг до приблизительно 150 мг/кг, от приблизительно 5 мг/кг до приблизительно 100 мг/кг, от приблизительно 10 мг/кг до приблизительно 100 мг/кг, или от приблизительно 10 мг/кг до приблизительно 60 мг/кг. Например, терапевтически эффективное количество вводят субъекту в дозе, по меньшей мере, приблизительно 0,05 мкг/кг, 0,2 мкг/кг, 0,5 мкг/кг, 1 мкг/кг, 10 мкг/кг, 100 мкг/кг, 0,2 мг/кг, 1,0 мг/кг, 2,0 мг/кг, 3,0 мг/кг, 5,0 мг/кг, 10 мг/кг, 25 мг/кг, 50 мг/кг массы тела или более.
В некоторых вариантах осуществления, терапевтически эффективное количество (1S,2S,3S,5R)-3-((6-(дифторметил)-5-фтор-1,2,3,4-тетрагидроизохинолин-8-ил)окси)-5-(4-метил-7H-пирроло-[2,3-d]пиримидин-7-ил)циклопентан-1,2-диола представляет собой дозу от приблизительно 1 мг/м2 до приблизительно 3000 мг/м2, от приблизительно 2 мг/м2 до приблизительно 2000 мг/м2, от приблизительно 3 мг/м2 до приблизительно 1000 мг/м2, от приблизительно 4 мг/м2 до приблизительно 750 мг/м2, от приблизительно 5 мг/м2 до приблизительно 600 мг/м2, от приблизительно 6 мг/м2 до приблизительно 550 мг/м2, от приблизительно 7 мг/м2 до приблизительно 500 мг/м2, от приблизительно 8 мг/м2 до приблизительно 450 мг/м2, от приблизительно 9 мг/м2 до приблизительно мг/м2. Например, терапевтически эффективное количество вводят субъекту в дозе, по меньшей мере, приблизительно 5 мг/м2, 10 мг/м2, 15 мг/м2, 20 мг/м2, 25 мг/м2, 30 мг/м2, 35 мг/м2, 40 мг/м2, 45 мг/м2, 50 мг/м2, 55 мг/м2, 60 мг/м2, 65 мг/м2, 70 мг/м2, 75 мг/м2, 80 мг/м2, 85 мг/м2, 90 мг/м2, 95 мг/м2, 100 мг/м2, 105 мг/м2, 110 мг/м2, 115 мг/м2, 120 мг/м2, 130 мг/м2, 135 мг/м2, 140 мг/м2, 145 мг/м2, 150 мг/м2, 155 мг/м2, 160 мг/м2, 165 мг/м2, 170 мг/м2, 175 мг/м2, 180 мг/м2, 185 мг/м2, 190 мг/м2, 195 мг/м2 или 200 мг/м2.
В некоторых вариантах осуществления, введение терапевтически эффективного количества (или дозы) описанных в изобретении соединений может быть проведено один раз в сутки (QD), два раза в сутки (BID), или при других режимах дозирования. В некоторых вариантах осуществления, суточная доза 16 мг может быть введена в форме одной суточной дозы 16 мг или в форме двух доз по 8 мг в сутки. В некоторых вариантах осуществления, суточная доза 6 мг может быть введена в форме одной суточной дозы 6 мг или в форме двух доз по 3 мг в сутки. В некоторых вариантах осуществления, лекарственный препарат вводят в течение периода или периодов времени 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 или 31 день. Введение может быть также проведено в течение более длительных периодов времени и может продолжаться в течение 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23 или 24 месяцев, или дольше.
Указанные в изобретении дозировки являются приблизительными, точная дозировка и частота введения зависят от конкретно используемой формы препарата (1S,2S,3S,5R)-3-((6-(дифторметил)-5-фтор-1,2,3,4-тетрагидроизохинолин-8-ил)окси)-5-(4-метил-7H-пирроло[2,3-d]-пиримидин-7-ил)циклопентан-1,2-диола или его фармацевтически приемлемой соли, тяжести подвергаемого лечению состояния, возраста, массы тела, общего состояния здоровья конкретного пациента, другого хорошо известного специалистам в данной области лекарственного средства, которое может принимать пациент, и могут быть более точно определены путем измерения уровня или концентрации (1S,2S,3S,5R)-3-((6-(дифторметил)-5-фтор-1,2,3,4-тетрагидроизохинолин-8-ил)окси)-5-(4-метил-7H-пирроло-[2,3-d]пиримидин-7-ил)циклопентан-1,2-диола или его фармацевтически приемлемой соли в крови субъекта и/или ответной реакции субъекта на проводимое лечения конкретного состояния.
В конкретных вариантах осуществления изобретения, количество (1S,2S,3S,5R)-3-((6-(дифторметил)-5-фтор-1,2,3,4-тетрагидро-изо-хинолин-8-ил)окси)-5-(4-метил-7H-пирроло-[2,3-d]пиримидин-7-ил)-циклопентан-1,2-диола или его фармацевтически приемлемой соли, используемое для лечения субъекта с аутоиммунным нарушением составляет меньшую величину или значительно меньшую величину (например, на >50% меньше), чем количество указанного соединения или его соли, которое необходимо для лечения рака. В силу этого, любые побочные эффекты и/или токсические явления, связанные с указанным соединением или его солью, сводятся до минимума и смягчаются.
Используемая в изобретении форма единственного числа включает также и форму множественного числа, если не указано иное. Например, заместитель включает один или более заместителей.
Термин "приблизительно", который используют в случае варьирования численно определенного параметра, означает, что параметр может изменяться не менее чем на 10% выше или ниже указанного числового значения для этого параметра. Например, следует иметь в виду, что доза, составляющая приблизительно 5 мг/кг, может варьировать в интервале от 4,5 мг/кг до 5,5 мг/кг, если не указано иное.
Термин "пациент" или "субъект" относится к любому взятому в отдельности субъекту, для которого требуется проведение терапии или который участвует в клиническом испытании, эпидемиологическом исследовании или которого используют в качестве контроля, включая людей и млекопитающих пациентов в ветеринарии, таких как крупный рогатый скот, лошади, собаки и кошки. В некоторых предпочтительных вариантах осуществления, субъектом является человек.
Используемый в изобретении термин "лечить" или "лечение" псориаза, системной красной волчанки (SLE) или любого другого аутоиммунного нарушения, состояния или заболевания означает применение терапии по настоящему изобретению в отношении субъекта, страдающего псориазом, системной красной волчанкой (SLE) или любым другим аутоиммунным нарушением, состоянием или заболеванием с целью достижения, по меньшей мере, одного положительного терапевтического эффекта, такого как, например, облегчение состояния или заболевания, уменьшение количества псориатических очагов поражения или снижение их тяжести, предотвращения нарушения или состояния, к которым применяется этот термин, или одного или более симптомов такого нарушения или состояния. Если не указано иное, то используемый в изобретении термин "лечение" относится к акту лечения в форме только что определенного выше "лечения". Термин "лечение" также включает адъювантное лечение и неоадъювантное лечение субъекта.
Термин "BID" (или "bid" или "b.i.d.") означает, что лекарственный препарат вводят дважды (два раза) в сутки. Например, 8 мг BID представляет суточную дозу 16 мг, вводимую в форме первой и второй дозы по 8 мг в сутки.
Термин "QD" (или "qd" или "q.d.") означает, что лекарственный препарат вводят однократно (один раз) в сутки.
Термины "схема лечения", "протокол дозирования" и "режим дозирования" используются взаимозаменяемо применительно к дозе и моменту времени введения каждого терапевтического средства в комбинации по изобретению.
"Улучшение" означает уменьшение или облегчение одного или нескольких симптомов при лечении с помощью описанной в изобретении комбинации по сравнению со случаем, когда комбинацию не применяют. "Улучшение" также включает сокращение или уменьшение продолжительности проявления симптома.
Используемые в настоящем изобретении термины "эффективное дозирование", "эффективная доза", "эффективное количество" или "терапевтически эффективное количество" лекарственного средства, соединения или фармацевтической композиции обозначают количество, достаточное для достижения одного или более положительных или требуемых эффектов в отношении биохимических, гистологических и/или поведенческих симптомов заболевания, их осложнений и промежуточных патологических фенотипов, проявляющихся в процессе развития заболевания. Для терапевтического применения, "терапевтически эффективное количество" относится к такому количеству вводимого соединения, которое позволит облегчить, в некоторой степени, один или несколько симптомов заболевания, подлежащего лечению. Эффективная доза может быть введена за одно или несколько введений. Применительно к настоящему изобретению, эффективная доза лекарственного средства, соединения или фармацевтической композиции представляет собой количество, достаточное для проведения прямого или косвенного профилактического или терапевтического лечения. С точки зрения применения в клинике, эффективная доза лекарственного средства, соединения или фармацевтической композиции может достигаться или не достигаться в случае использования в комбинации с другим лекарственным средством, соединением или фармацевтической композицией.
"Фармацевтически приемлемые" относятся к тем свойствам и/или веществам, которые приемлемы для пациента с фармакологической/токсикологической точки зрения и для химика-фармацевта-производителя с физической/химической точки зрения в отношении композиции, лекарственной формы, стабильности, приемлемости и биодоступности для пациента.
В случае, когда приводятся данные по растворимости твердого вещества в растворителе, отношение твердого вещества к растворителю выражают как масса/объем (м/о).
В случае, когда указывается % активного ингредиента в фармацевтической композиции, этот процент представляет собой отношение активного ингредиента ко всей фармацевтической композиции в целом и выражается как масса/масса (м/м).
(1S,2S,3S,5R)-3-((6-(дифторметил)-5-фтор-1,2,3,4-тетра-гидроизохинолин-8-ил)окси)-5-(4-метил-7H-пирроло[2,3-d]-пиримидин-7-ил)циклопентан-1,2-диол относится к соединению:
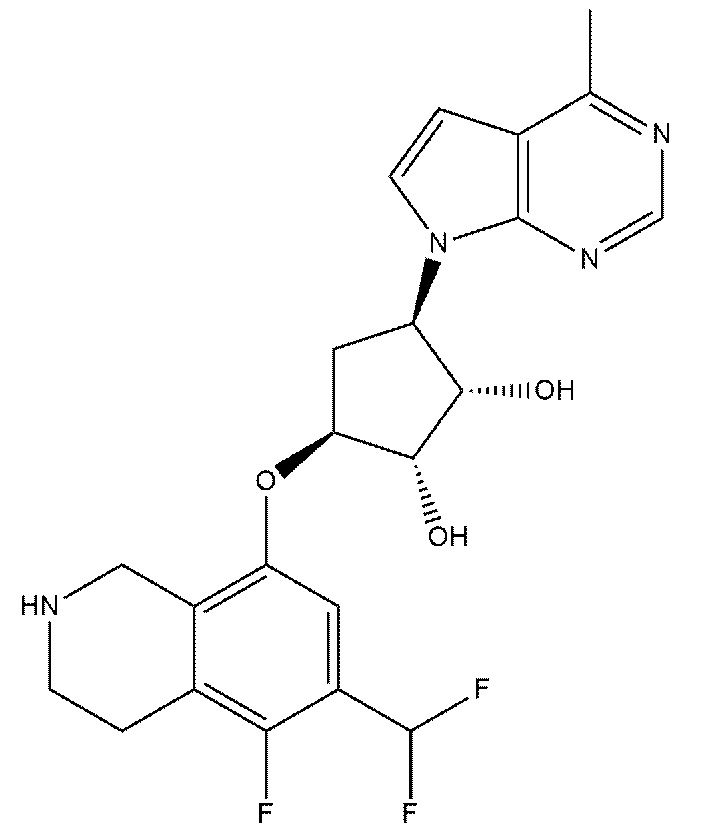
Фармацевтически приемлемые соли (1S,2S,3S,5R)-3-((6-(дифторметил)-5-фтор-1,2,3,4-тетрагидроизохинолин-8-ил)окси)-5-(4-метил-7H-пирроло[2,3-d]пиримидин-7-ил)циклопентан-1,2-диола включают ацетатные, аспартатные, бензоатные, безилатные, бикарбонатные /карбонатные, бисульфатные/сульфатные, боратные, камзилатные, цитратные, эдизилатные, эзилатные, формиатные, фумаратные, глюцептатные, глюконатные, глюкуронатные, гексафторфосфатные, гибензатные, гидрохлоридные/хлоридные, гидробромидные/бромидные, гидройодидные/йодидные, изетионатные, лактатные, малатные, малеатные, малонатные, мезилатные, метилсульфатные, нафтилатные, 2-напсилатные, никотинатные, нитратные, оротатные, оксалатные, пальмитатные, памоатные, фосфатные/гидрофосфатные/дигидрофосфатные, сахаратные, стеаратные, сукцинатные, тартратные, тозилатные и трифторацетатные соли, соли алюминия, аргинина, бензатина, кальция, холина, диэтиламина, диоламина, глицина, лизина, магния, меглюмина, оламина, калия, натрия, трометамина, тозилата и цинка. Обзор подходящих солей можно найти в руководстве "Handbook of Pharmaceutical Salts: Properties, Selection, and Use” by Stahl and Wermuth (Wiley-VCH, Weinheim, Germany, 2002), полное содержание которого включено в настоящее изобретение путем ссылки на него.
Синтез (1S,2S,3S,5R)-3-((6-(дифторметил)-5-фтор-1,2,3,4-тетрагидроизохинолин-8-ил)окси)-5-(4-метил-7H-пирроло[2,3-d]-пиримидин-7-ил)циклопентан-1,2-диола описан в Патенте США № 10220037, принадлежащем заявителю настоящего изобретения, полное содержание которого включено в настоящее изобретение путем ссылки на него. Кроме того, кристаллические формы 1S,2S,3S,5R)-3-((6-(дифторметил)-5-фтор-1,2,3,4-тетрагидроизохинолин-8-ил)окси)-5-(4-метил-7H-пирроло[2,3-d]пиримидин-7-ил)циклопентан-1,2-диола описаны в патентном документе PCT Publication No. WO2020152557, принадлежащем заявителю настоящего изобретения, полное содержание которого включено в настоящее изобретение путем ссылки на него.
ПРИМЕРЫ
Предполагается, что специалист в данной области может в результате ознакомления с приведенным выше описанием и не проводя дополнительных исследований применить на практике настоящее изобретение в его наиболее полном объеме. В приведенных далее подробных примерах описывается получение различных соединений и/или осуществление способов по изобретению, и эти примеры следует рассматривать только как иллюстрации, но они никоим образом не являются ограничениями для настоящего изобретения. Для специалистов в данной области техники является очевидным, что могут быть внесены соответствующие изменения в осуществление методик проведения эксперимента, как в отношении реагентов, так и в отношении условий и методов проведения реакций.
ПРИМЕР 1. Облегчение симптомов псориаза у белого мужчины в возрасте 61 года
Пациент, белый мужчина в возрасте 61 года, страдал тяжелой формой псориаза в течение 4-5 лет. У него были хронические очаги псориатического поражения на передней и задней сторонах торса. Очаги поражения покрывали 75% его тела, и пациенту было трудно бороться с проявлениями этих симптомов, несмотря на то, что ранее он принимал несколько разных лекарственных препаратов. Симптомы псориаза ухудшались после проведения химиотерапии.
Проводили лечение пациента путем перорального введения два раза в сутки в течение четырех месяцев 1 мг (1S,2S,3S,5R)-3-((6-(дифторметил)-5-фтор-1,2,3,4-тетрагидроизохинолин-8-ил)-окси)-5-(4-метил-7H-пирроло[2,3-d]пиримидин-7-ил)циклопентан-1,2-диола.
В течение периода лечения, пациента опрашивали о других болезненных состояниях, если таковые имелись, которые он тогда испытывал. В ответ пациент указал, что он испытал улучшение состояние псориатических поражений кожи и уменьшение связанного с этим зуда через одну неделю после начала лечения. Кроме того, у пациента наблюдалось значительное уменьшение очагов псориатического поражения кожи после шестинедельного лечения. Пациент прекратил лечение через четыре месяца по причинам, не связанным с псориазом. Через месяц после прекращения лечения, псориатические поражения кожи пациента оставались в стадии ремиссии. Во время лечения, им не использовались никакие другие методы лечения псориаза. Фотографии, сделанные после двух и шести недель лечения, свидетельствуют об устранении симптомов псориаза. На фигурах 1 и 2 показано отсутствие симптомов псориаза.
Полное содержание всех цитируемых в изобретении публикаций и патентных заявок включено в настоящее изобретение путем ссылок на них. Несмотря на то, что представленное выше изобретение было описано довольно подробно посредством иллюстраций и примеров, тем не менее, для обычных специалистов в данной области является очевидным, что на основе идей этого изобретения могут быть сделаны конкретные изменения и модификации, не отступая при этом от сущности или объема изобретения, определяемых прилагаемой формулы изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПОЛИМОРФНАЯ ФОРМА СОЛИ ГИДРАТА МОНОФОСФАТА ИЗВЕСТНОГО ПРОИЗВОДНОГО ТЕТРАГИДРОИЗОХИНОЛИНА | 2020 |
|
RU2801355C2 |
| ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ КАРБОНУКЛЕОЗИДА, ПРИМЕНЯЕМЫЕ В КАЧЕСТВЕ ПРОТИВОРАКОВЫХ АГЕНТОВ | 2017 |
|
RU2712944C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМБИНАЦИЯ НА ОСНОВЕ ИНГИБИТОРОВ PRMT5 | 2020 |
|
RU2830439C1 |
| ИНГИБИТОРЫ RMT5 | 2019 |
|
RU2814198C2 |
| ЛЕЧЕНИЕ ГИДРАДЕНИТА ИНГИБИТОРАМИ JAK | 2020 |
|
RU2805595C1 |
| СОЕДИНЕНИЯ И КОМПОЗИЦИИ, ПРИМЕНЯЕМЫЕ ДЛЯ ЛЕЧЕНИЯ РАССТРОЙСТВ, СВЯЗАННЫХ С NTRK | 2016 |
|
RU2744974C2 |
| ЗАМЕЩЕННЫЕ ПУРИНОВЫЕ И 7-ДЕАЗАПУРИНОВЫЕ СОЕДИНЕНИЯ | 2011 |
|
RU2606514C2 |
| ПРОИЗВОДНЫЕ 5-(7Н-ПИРРОЛО[2,3-d]ПИРИМИДИН-4-ИЛ)-5-АЗАСПИРО[2.5]ОКТАН-8-КАРБОНОВОЙ КИСЛОТЫ В КАЧЕСТВЕ НОВЫХ ИНГИБИТОРОВ JAK-КИНАЗЫ | 2018 |
|
RU2761626C2 |
| МОДУЛЯТОРЫ MAS-СВЯЗАННОГО РЕЦЕПТОРА G-БЕЛКА X2 И СВЯЗАННЫЕ С НИМИ ПРОДУКТЫ И СПОСОБЫ | 2021 |
|
RU2841536C1 |
| КОМПОЗИЦИИ И СПОСОБЫ ИНГИБИРОВАНИЯ ВИРУСНОЙ ПОЛИМЕРАЗЫ | 2013 |
|
RU2654482C2 |

Изобретение относится к области медицины, а именно к способу лечения аутоиммунного нарушения. Предлагается способ лечения субъекта, страдающего от аутоиммунного нарушения, включающий введение указанному субъекту, нуждающемуся в этом, терапевтически эффективного количества ингибитора PRMT5, где ингибитор PRMT5 представляет собой (1S,2S,3S,5R)-3-((6-(дифторметил)-5-фтор-1,2,3,4-тетрагидроизо-хинолин-8-ил)окси)-5-(4-метил-7H-пирроло[2,3-d]пиримидин-7-ил)-циклопентан-1,2-диол:
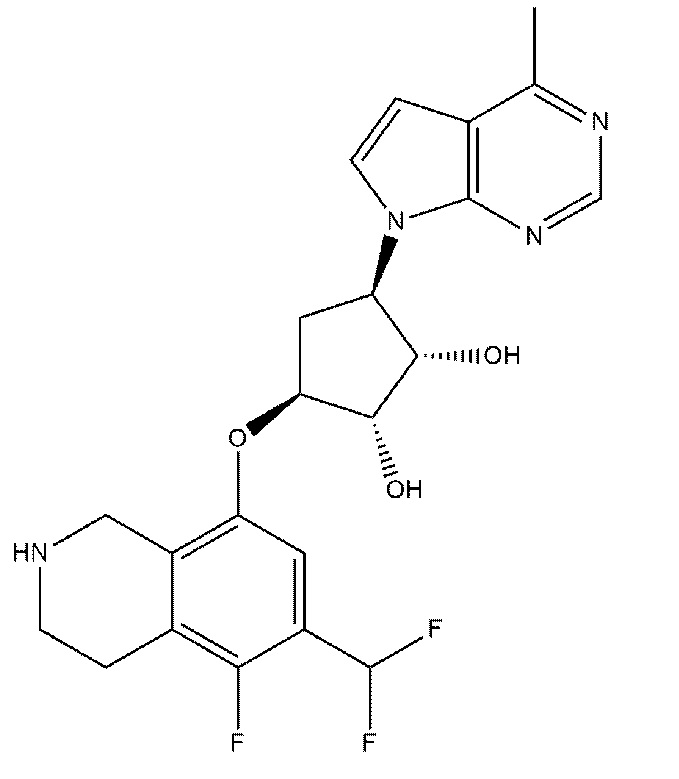
или его фармацевтически приемлемую соль, где указанному субъекту вводят терапевтически эффективное количество от 0,5 мг до 120 мг. Использование способа эффективно для лечения аутоиммунного нарушения, в частности, такого как псориаз. 20 з.п. ф-лы, 1 пр., 4 ил.
1. Способ лечения субъекта, страдающего от аутоиммунного нарушения, включающий введение указанному субъекту, нуждающемуся в этом, терапевтически эффективного количества ингибитора PRMT5, где ингибитор PRMT5 представляет собой (1S,2S,3S,5R)-3-((6-(дифторметил)-5-фтор-1,2,3,4-тетрагидроизо-хинолин-8-ил)окси)-5-(4-метил-7H-пирроло[2,3-d]пиримидин-7-ил)-циклопентан-1,2-диол или его фармацевтически приемлемую соль;
где указанному субъекту вводят терапевтически эффективное количество от приблизительно 0,5 мг до приблизительно 120 мг.
2. Способ по п. 1, где аутоиммунное нарушение выбирают из группы, состоящей из псориаза, атопического дерматита, очаговой алопеции, анкилозирующего спондилита, астмы, сахарного диабета I типа, множественного склероза, целиакии, склеродермии, гнойного гидраденита, витилиго, дерматомиозита, системной красной волчанки, ревматоидного артрита, псориатического артрита и воспалительного заболевания кишечника.
3. Способ по п. 2, где аутоиммунное нарушение представляет собой псориаз.
4. Способ по любому одному из предшествующих пунктов, где указанное терапевтически эффективное количество вводят энтерально, парентерально или местно.
5. Способ по п. 4, где указанное энтеральное введение проводят перорально или ректально.
6. Способ по п. 5, где указанное пероральное введение осуществляют в форме таблетки, капсулы или в жидкой лекарственной форме.
7. Способ по п. 4, где указанное парентеральное введение проводят внутривенно или внутрисуставно.
8. Способ по п. 4, где указанное местное введение осуществляют в форме раствора, крема, мази, геля, лосьона, суспензии или эмульсии.
9. Способ по п.1, где указанное терапевтически эффективное количество выбирают из группы, состоящей из приблизительно 0,5 мг, 1 мг, 2 мг, 4 мг, 6 мг, 8 мг, 10 мг, 16 мг, 32 мг, 60 мг, 80 мг и 120 мг.
10. Способ по п. 9, где указанное терапевтически эффективное количество составляет приблизительно 12 мг.
11. Способ по п. 9, где указанное терапевтически эффективное количество составляет приблизительно 10 мг.
12. Способ по п. 9, где указанное терапевтически эффективное количество составляет приблизительно 8 мг.
13. Способ по п. 9, где указанное терапевтически эффективное количество составляет приблизительно 6 мг.
14. Способ по п. 9, где указанное терапевтически эффективное количество составляет приблизительно 4 мг.
15. Способ по п. 9, где указанное терапевтически эффективное количество составляет приблизительно 1 мг.
16. Способ по любому одному из пп. 1-15, где указанное терапевтически эффективное количество вводят один раз в сутки (QD).
17. Способ по любому одному из пп.1-15, где указанное терапевтически эффективное количество вводят два раза в сутки (BID).
18. Способ по любому одному из пп.1-17, где указанный (1S,2S,3S,5R)-3-((6-(дифторметил)-5-фтор-1,2,3,4-тетрагидроизо-хинолин-8-ил)окси)-5-(4-метил-7H-пирроло[2,3-d]пиримидин-7-ил)-циклопентан-1,2-диол или его фармацевтически приемлемую соль вводят в течение от 1 до 28 дней.
19. Способ по любому одному из пп. 1-17, где указанный (1S,2S,3S,5R)-3-((6-(дифторметил)-5-фтор-1,2,3,4-тетрагидроизо-хинолин-8-ил)окси)-5-(4-метил-7H-пирроло[2,3-d]пиримидин-7-ил)-циклопентан-1,2-диол или его фармацевтически приемлемую соль вводят в течение 1-6 недель.
20. Способ по любому одному из пп. 1-17, где указанный (1S,2S,3S,5R)-3-((6-(дифторметил)-5-фтор-1,2,3,4-тетрагидроизо-хинолин-8-ил)окси)-5-(4-метил-7H-пирроло[2,3-d]пиримидин-7-ил)-циклопентан-1,2-диол или его фармацевтически приемлемую соль вводят в течение 1-6 месяцев.
21. Способ по п.20, где указанный (1S,2S,3S,5R)-3-((6-(дифторметил)-5-фтор-1,2,3,4-тетрагидроизо-хинолин-8-ил)окси)-5-(4-метил-7H-пирроло[2,3-d]пиримидин-7-ил)-циклопентан-1,2-диол или его фармацевтически приемлемую соль вводят в течение 1-4 месяцев.
| Способ получения цианистых соединений | 1924 |
|
SU2018A1 |
| Станок для придания концам круглых радиаторных трубок шестигранного сечения | 1924 |
|
SU2019A1 |
| US 10220037 B2, 05.03.2019 | |||
| Приспособление для впрыскивания горючего в двигателях внутреннего горения | 1930 |
|
SU27908A1 |
| WEBB LINDSAY M | |||
| et al | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
| J Immunol | |||
| Автомобиль-сани, движущиеся на полозьях посредством устанавливающихся по высоте колес с шинами | 1924 |
|
SU2017A1 |
| Складная решетчатая мачта | 1919 |
|
SU198A1 |
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Прибор для нейтрализации отработанных газов | 1922 |
|
SU1439A1 |
| [онлайн], [найдено 27.02.2023] | |||
| Найдено в PubMed, | |||
Авторы
Даты
2023-09-11—Публикация
2021-01-04—Подача