Изобретение относится к получению солей циркония из карбоновых кислот, в частности к соли четырехвалентного циркония и муравьиной кислоты. Карбоксилаты циркония относятся к новому классу металлорганических каркасов и применяются в качестве основы катализаторов различных химических процессов, при получении металлсодержащих полимеров, при получении керамических материалов в микроэлектронике, солнечной энергетике, элементов производства и накопления энергии и покрытий на основе ZrO2, красителей, пигментов, в качестве присадок к индустриальным маслам и другим смазочным материалам.
Известен способ получения карбоксилата циркония, в частности, металлорганического каркаса на основе циркония и бензол-1,4-дикарбоновой кислоты в условиях СВЧ активации. В качестве соли циркония используют оксихлорид циркония формулы ZrOCl2×8H2O, а в качестве растворителя используют ледяную уксусную кислоту, нагрев реакционной смеси осуществляют под воздействием СВЧ излучения мощностью до 200 Вт и частотой 2,465 ГГц при атмосферном давлении (патент RU 2784345; МПК C07F 7/00, H05B 6/64, B01J 20/02, B01J 20/26, B01J 20/28, B01J 20/30, B01J 32/00; 2022 год).
Недостатками известного способа являются синтез при повышенной температуре (120°С) в среде агрессивной ледяной уксусной кислоты, необходимость отмывки продукта высокотоксичным метанолом и активации на вакууме в течение 8 часов.
Известен способ получения карбоксилатов циркония взаимодействием четыреххлористого циркония ZrCl4 с карбоксильными производными общей формулы RCOOM, где R – линейный или разветвленный алифатический радикал CnH2n+1 или остаток ненасыщенной кислоты, где n=0-16, а М – протон или катион щелочного металла. Механическую активацию смеси проводят в реакторе из нержавеющей стали с использованием в качестве активирующей насадки стальных шаров диаметром 5-15 мм на эксцентриковой шаровой вибрационной мельнице с рабочей частотой 5-50 Гц и амплитудой 5-20 мм при температуре 10-40°С в течение 15-180 мин при соотношении массы активирующей насадки к массе полезной загрузки в пределах (50-150):1. Процесс проводят в атмосфере инертного газа (патент RU 2332398; МПК C07C 51/41; C07C 53/124; C07C 53/126; C07C 53/10; C07C 7/03; C07F 7/00: 2008 год).
Недостатки способа: необходимость проведения предварительной активации, либо длительно, либо при высокой температуре, поскольку синтез проводят в твердой фазе; для отделения продукта из реакционной смеси необходимо проведение стадии экстракции в токсичном органическом растворителе – толуоле, который нужно удалять отгонкой; использование относительно дорогого и токсичного реагента – тетрахлорида циркония и главное – получение загрязненного ионами хлора продукта.
Известен способ получения Zr-оксо-кластера с монокарбоксилатным (формиатным) лигандом, в соответствии с которым продукт [Zr6O4(OH)4(HCOO)12]·DMF·6H2O синтезирован в виде бесцветных пластиноподобных кристаллов в результате сольвотермической реакции между хлоридом циркония ZrCl4, муравьиной кислотой и 3,5-пиридиндикарбоновой кислотой или 2,4-пиридиндикарбоновой кислотой в среде N,N'-диметилформамида (DMF) при 100°C в течение 72 ч (Liang W., Babarao R., Murphy M.J., D'Alessandro D.M. The first example of a zirconium-oxide based metal-organic framework constructed from monocarboxylate ligands. Dalton Trans. 44(4) (2015)1516-9).
Недостатками метода являются использование токсичных реагентов, высокая температура и большая продолжительность синтеза. Кроме того, в качестве конечного продукта получают сольват ZrO0.67(OH)0.67(HCOO)2·DMF·H2O, содержащий N,N'-диметилформамид.
Наиболее близким к заявленному изобретению (прототип) является способ получения формиата циркония путем кипячения хлорида циркония в предварительно обезвоженной муравьиной кислоте (98%) в течение 4-5 ч до удаления газообразного HCl, отделения кристаллического продукта фильтрованием, промывкой дихлорметаном от ионов хлора и сушкой при пониженном давлении (Paul R.C., Baidya O.B., Kapoor R. Zirconium and oxozirconium (IV) formates, Z. Naturforsch. 31b (1975) 300-303).
Недостатками метода являются необходимость предварительного получения безводной муравьиной кислоты, применение токсичных реагентов – тетрахлорида циркония и дихлорметана, используемого для удаления остатков хлорид-ионов при промывке, и сушка продукта при пониженном давлении.
Таким образом, перед авторами стояла задача разработать аппаратурно- и технологически простой способ получения формиата циркония без использования токсичных реагентов.
Поставленная задача решена в предлагаемом способе получения формиата циркония, включающем взаимодействие неорганической соли циркония и концентрированной муравьиной кислоты, в котором предварительно пентагидрат гидроксокарбоната циркония состава Zr(OH)2CO3×5H2O растворяют в 60-70 %-ной азотной кислоте, взятых при соотношении порошок соли : кислота = 1 : (10-15), и выдерживают при температуре 50-70°С до получения сухого остатка, полученный сухой остаток растворяют в 85% муравьиной кислоте, взятой в соответствии со стехиометрией, и выдерживают при комнатной температуре до завершения спонтанно возникающей реакции с получением осадка в виде белого кристаллического порошка.
В настоящее время из научно-технической и патентной литературы не известен способ получения формиата циркония, включающий предварительное получение нитрата циркония состава ZrO(NO3)2 путем растворения пентагидрата гидроксокарбоната циркония состава Zr(OH)2CO3×5H2O в 60-70 % азотной кислоте при соотношении порошок соли : кислота = 1 : (10-15) и выдержкой при температуре 50-70°С до получения сухого остатка с последующим его взаимодействием с муравьиной кислотой.
Исследования, проведенные авторами, позволили разработать способ получения формиата циркония ZrO(HCOO)2·2H2O, обеспечивающий технологическую простоту наряду с несложным аппаратурным оформлением. Способ дает возможность использования муравьиной кислоты, взятой в стехиометрическом количестве. Проведение процесса без нагревания обусловлено спонтанным экзотермическим взаимодействием нитрата циркония ZrO(NO3)2 с 85% муравьиной кислотой HCOOH при их смешивании. Технологическая простота способа обеспечивается использованием нитрата циркония ZrO(NO3)2 в качестве источника циркония (IV), который хорошо растворяется в муравьиной кислоте при комнатной температуре.
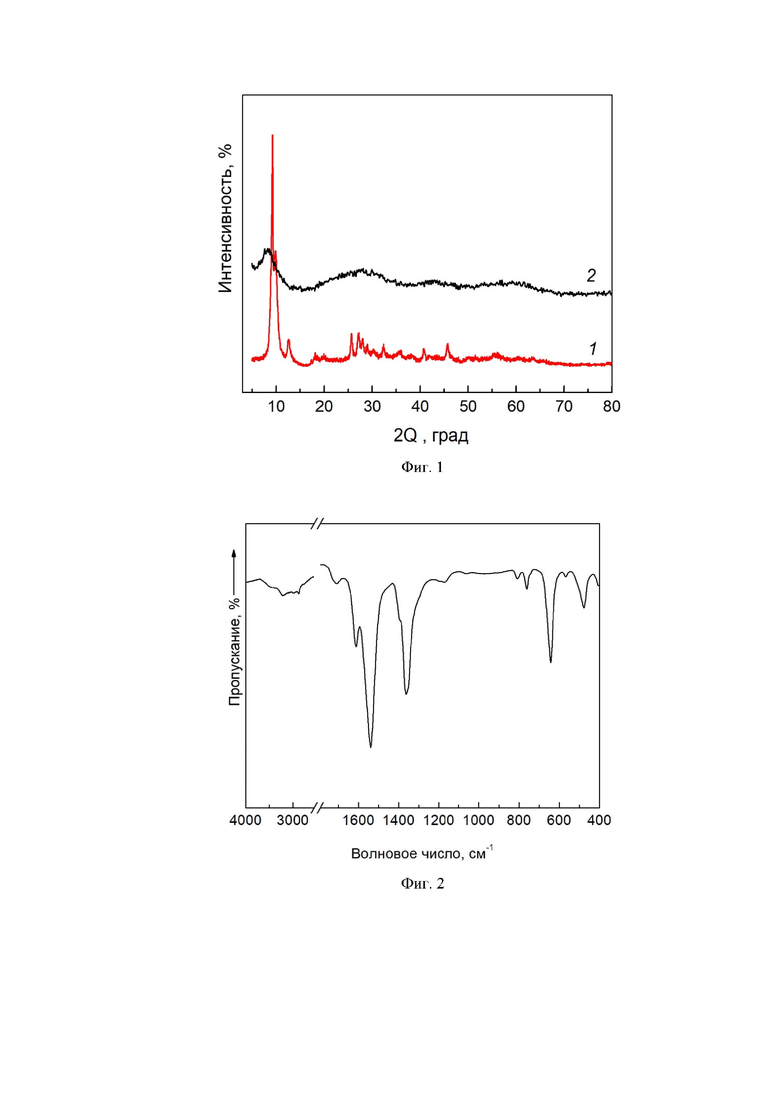
Предлагаемый способ может быть осуществлен следующим образом: влажные соли или порошок нитрата циркония состава ZrO(NO3)2, полученного прямым воздействием 60-70 % азотной кислоты HNO3 на пентагидрат гидроксокарбоната циркония Zr(OH)2CO3×5H2O при соотношении порошок соли : кислота = 1 : (10-15) и выдержке при температуре 50-70°С до получения сухого остатка, растворяют в муравьиной кислоте (85 % HCOOH), взятой в соответствии со стехиометрией, и выдерживают при комнатной температуре до завершения спонтанно возникающей реакции с получением осадка в виде белого кристаллического порошка. Полученный продукт аттестуют рентгенофазовым анализом (РФА) и ИК спектроскопией. По результатам РФА и ИК-спектроскопии кристаллический продукт представляет собой формиат циркония ZrO(HCOO)2×2H2O. Согласно данным СЭМ ZrO(HCOO)2×2H2O имеет вид склонных к агломерированию пластинчатых белых кристаллов со средним размером 200×500 нм. Отличительной особенностью полученного формиата циркония является его растворимость в воде с образованием истинного раствора. После испарения воды происходит образование рентгеноаморфной прозрачной пленки вследствие полимеризации формиата без обратной кристаллизации (фиг. 1, линия 2), что подтверждает его индивидуальность и отсутствие других кристаллических фаз, а также позволяет его использование в последующем для получения тонкопленочных материалов и покрытий на основе циркония.
На Фиг. 1 приведены дифрактограммы образцов ZrO(HCOO)2×2H2O исходного (1) и после растворения в воде (2).
На Фиг. 2. приведены ИК-спектры образца ZrO(HCOO)2×2H2O.
На Фиг. 3. приведено СЭМ изображения образца ZrO(HCOO)2×2H2O.
Предлагаемый способ иллюстрируется следующими примерами:
Пример 1. Порошок пентагидрата гидроксокарбоната циркония Zr(OH)2CO3×5H2O (2 г) помещают в термостойкий стакан и растворяют в 20 мл 70% азотной кислоты HNO3 (конц.), что соответствует соотношению порошок соли : кислота = 1 : 10. Упаривают до сухого остатка (влажных солей нитрата циркония) при нагревании при 50°С в течение 30 мин постепенно. Влажный порошок нитрата циркония растворяют в стехиометрическом количестве 85% муравьиной кислоты HCOOH при комнатной температуре. После полного растворения влажных солей взаимодействие начинается быстро (в течение 5-10 минут) с сильным разогревом, с выделением оксидов азота и образованием кристаллов белого цвета. По данным РФА и ИК-спектроскопии кристаллический продукт является формиатом циркония ZrO(HCOO)2×2H2O (см. Фиг. 2). Согласно данным СЭМ ZrO(HCOO)2×2H2O имеет вид склонных к агломерированию пластинчатых белых кристаллов со средним размером 200×500 нм (см. Фиг. 3). Полученный порошок легко растворяется в воде с образованием прозрачного раствора.
Пример 2. Порошок пентагидрата гидроксокарбоната циркония Zr(OH)2CO3×5H2O (5 г) помещают в термостойкий стакан и растворяют в 75 мл 60%-ной HNO3 (конц.), что соответствует соотношению порошок соли : кислота = 1 : 15. Упаривают до сухого остатка (влажных солей нитрата циркония) при нагревании при 70°С в течение 20 мин постепенно. Влажный порошок нитрата циркония растворяют в стехиометрическом количестве 85% муравьиной кислоты HCOOH при комнатной температуре. После полного растворения влажных солей взаимодействие начинается быстро (в течение 5-10 мин) с сильным разогревом, с выделением оксидов азота и образованием кристаллов белого цвета. По данным РФА и ИК-спектроскопии кристаллический продукт является формиатом циркония ZrO(HCOO)2×2H2O (см. Фиг. 2). Согласно данным СЭМ ZrO(HCOO)2×2H2O имеет вид склонных к агломерированию пластинчатых белых кристаллов со средним размером 200×500 нм (см. Фиг. 3). Полученный порошок легко растворяется в воде с образованием прозрачного раствора.
Таким образом, предлагается аппаратурно- и технологически простой способ получения формиата циркония без использования токсичных реагентов.
| название | год | авторы | номер документа |
|---|---|---|---|
| Металлоорганический каркасный материал и способ получения оксида циркония, допированного скандием, с его использованием | 2024 |
|
RU2837917C1 |
| Способ получения формиата меди (II) | 2019 |
|
RU2702227C1 |
| Способ получения двойного молибдата циркония-натрия | 2021 |
|
RU2772529C1 |
| Ниобий-замещенный молибдат натрия-циркония и способ его получения | 2023 |
|
RU2814778C1 |
| Сложный молибдат натрия-висмута-циркония | 2023 |
|
RU2807408C1 |
| Способ получения формиата железа (II) | 2018 |
|
RU2670440C1 |
| Способ получения формиата алюминия | 2024 |
|
RU2836145C1 |
| БЫСТРЫЙ И МАСШТАБИРУЕМЫЙ СПОСОБ ПОЛУЧЕНИЯ МИКРОПОРИСТОГО ТЕРЕФТАЛАТА ЦИРКОНИЯ(IV) | 2019 |
|
RU2719597C1 |
| Способ получения нанокристаллического сложного оксида иттрия | 2023 |
|
RU2819497C1 |
| Двойной молибдат натрия-висмута и способ его получения | 2022 |
|
RU2775986C1 |

Изобретение относится к способу получения формиата циркония. Предложенный способ включает взаимодействие неорганической соли циркония и концентрированной муравьиной кислоты. При этом предварительно пентагидрат гидроксокарбоната циркония состава Zr(OH)2CO3×5H2O растворяют в 70%-ной азотной кислоте при массовом соотношении порошок соли : кислота = 1 : 14 и выдерживают при температуре 50°С до получения сухого остатка, полученный сухой остаток растворяют в 85%-ной муравьиной кислоте, взятой в соответствии со стехиометрией, и выдерживают при комнатной температуре до завершения спонтанно возникающей реакции с получением осадка в виде белого кристаллического порошка. Техническим результатом изобретения является разработка аппаратурно- и технологически простого способа получения формиата циркония без использования токсичных реагентов. 3 ил., 2 пр.
Способ получения формиата циркония, включающий взаимодействие неорганической соли циркония и концентрированной муравьиной кислоты, отличающийся тем, что предварительно пентагидрат гидроксокарбоната циркония состава Zr(OH)2CO3×5H2O растворяют в 70%-ной азотной кислоте при массовом соотношении порошок соли : кислота = 1 : 14 и выдерживают при температуре 50°С до получения сухого остатка, полученный сухой остаток растворяют в 85%-ной муравьиной кислоте, взятой в соответствии со стехиометрией, и выдерживают при комнатной температуре до завершения спонтанно возникающей реакции с получением осадка в виде белого кристаллического порошка.
| PAUL R.CH | |||
| et al., Zirconium and Oxozirconium(IV) Formates, Zeitschrift fur Naturforschung Teil B, 1976, 31, p | |||
| ТКАЦКИЙ СТАНОК | 1920 |
|
SU300A1 |
| СПОСОБ ПОЛУЧЕНИЯ КАРБОКСИЛАТОВ ЦИРКОНИЯ | 2006 |
|
RU2332398C1 |
| LIANG W | |||
| et al., The first example of a zirconium-oxide based metalorganic framework constructed from monocarboxylate ligands, Dalton Trans., 2015, v | |||
| Приспособление для плетения проволочного каркаса для железобетонных пустотелых камней | 1920 |
|
SU44A1 |
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Способ извлечения канифоли из осмола | 1916 |
|
SU1516A1 |
| СПОСОБ ПОЛУЧЕНИЯ РАСТВОРОВ КАРБОКСИЛАТОВ ЦИРКОНИЯ | 2020 |
|
RU2750251C1 |
Авторы
Даты
2025-03-03—Публикация
2024-06-04—Подача