Изобретение относится к молекулярной биологии и генноинженерной биотехнологии и касается получения ДНК, кодирующей часть поверхностного белка CD4 Т-лимфо- цитов человека, ответственную за связывание с гликопротеином др 120 вируса иммунодефицита человека (ВИЧ), и ее фрагментов, продукты экспрессии которых могут найти применение при исследовании молекулярных механизмов развития синдрома приобретенного иммунодефицита человека (СПИД), диагностики ВИЧ, терапии и профилактики СПИД.
Известна кДНК, полученная из природной мРНК, кодирующая 374 аминокислотных остатка (АКО) N-концевой области поверхностного белка CD4 Т-лимфоцитов человека, ответственной за связывание с гликопротеином др 120 ВИЧ.
Недостатком данной ДНК является наличие участков, кодирующих фрагменты белка CD4, функционально незначащих для связывания с гликопротеином др120 ВИЧ, поскольку известно, что наиболее важной для связывания является область CD4 с 1 по 106 АКО, с З7 по 83, с 41 по 55, с 40 по 60, с 36 по 49 и с 81 по 92, существенна для связывания также область с 83 по 159 АКО; отсутствие удобных сайтов рестрикции для уменьшения ее размера.
Известны фрагменты кДНК, полученной из природной мРНК, кодирующие полипептиды N-концевой области CD4 протяженностью 388, 351, 152 АКО.
Недостатки ДНК, кодирующих первые два полипептида, также заключаются в избыточной протяженности. Недостатки ДНК, кодирующих полипептид протяженностью 152 АКО состоят в том,что они значительно перекрывают участок, минимально необходимый для связывания др120 и в то же время не включают весь фрагмент, взаимодействующий с др120.
Известны также фрагмент кДНК, кодирующий полипептид IM-концееого района CD4 протяженностью 113 АКО. соответствующий последовательности первого домена и междоменного участка белка.
Недостатками известного фрагмента являются, во-первых, его кодоновый состав, нехарактерный для прокариотов вообще и Е.соМ в частности, во-вторых, отсутствие сайтов рестрикции, позволяющих уменьшить их размер для локализации минимального фрагмента связывания белка др120.
Наиболее близкими по сущности и достигаемому результату являются фрагменты кДНК, кодирующие полипептиды N-конце- еой области CD4 протяженностью с -23 по
374, с 1 по 111, с 112 по 181, с 287 по 374, и с 182 по 286 АКО.
Общими недостатками этих фрагментов являются: неоптимальный кодоновый состав для экспрессии в прокариотических организмах и, в частности, в E.coli; неоптимальный, избыточный размер фрагментов: фрагмент 1-111 кодирует сразу оба центра связывания с белком др120, послед0 ние два из заявленных фрагментов кодируют полипептиды 287-374 и 182-286, несущественные для связывания с белком др120, а первый фрагмент кодирует полипептид -23-374, соответствующий всей
5 растворимой части белка CD4, включающей в себя протяженные области-23-0 и 182-374, также несущественные для связывания. В то же время отсутствуют удобные сайты рестрикции для генноинженерных манипуля0 ций, позволяющих уменьшить размер фрагментов до оптимальных величин, определяемых размерами центров связывания белка CD4. Неоптимальный кодоновый состав для экспрессии в прокариотах и отсут5 ствие достаточного количества удобных сайтов рестрикции обусловлено происхождением фрагментов изкДНК-копии мРНК эукариотического (человеческого) гена CD4.
0Целью настоящего изобретения является получение синтетической ДНК, кодирующей часть поверхностного белка CD4 Т-лимфоцитов человека, ответственную за связывание с гликопротеином др120 вируса
5 иммунодефицита человека, кодоновый состав которой оптимизирован для Escherichia coli.
Поставленная цель достигается получением синтетической ДНК abc с оптимизиро0 ванным для Escherichia coli кодоновым составом, кодирующей область ABC: 1-185 поверхностного белка CD4 Т-лимфоцитов человека, ответственную за связывание с гликопротеином др120 вируса иммунодефи5 цита человека, и ее фрагментов а, Ь, с, ab, кодирующих соответственно области CD4: А: 1-60, В: 59-110, С: 109-185, АВ: 1-110.
Фрагмент abc кодирует два N-концевых домена CD4, субфрагмент а - первый центр
0 связывания с гликопротеином др120 ВИЧ, субфрагмент b - второй центр связывания, субфрагмент с - второй домен белка CD4, субфрагмент ab - оба центра связывания. Ниже приведены нуклеотидные последова5 тельности фрагментов а.Ь.с и фрагментов ab и abc.
Изобретение осуществляется следующим образом. Твердофазным автоматическим фосфитамидным методом синтезируют олигодезоксирибочуклеотиды
(1-16), выходы и свойства синтетических олигодезоксирибонуклеотидов (1-16) представлены в таблице.
Олигодезоксирибонуклеотиды (2,3.5.7- 10.12,14,15) фосфорилируют АТФ по 5 -концу с помощью полинуклеотидкиназы (ПНК) фага Т4. Соединения (1-3, 9-11) или (4,5,12,13) или (6-8, 14-16) смешивают в эквимолекулярных соотношениях, нагревают при 95°С в течение 5 мин, охлаждают до комнатной температуры в течение 3 ч, проводят межнуклеотидную сшивку ДНК-лига- зой фага Т4. Продукты соответствующих длин выделяют электрофорезом в ПААГ, получают Фрагменты (а) или (Ь) или (с) соответственно.
Фрагмент (а) смешивают с векторной ДНК плазмиды pUC19, предварительно рес- щепленной рестриктазами Pst1 и Kpn1, a фрагменты (Ь) или (с) - с векторной ДНК плазмиды pUC18, расщепленной теми же рестриктазами, обрабатывают ДНК-лигазой фага Т4. Полученными смесями трансформируют клетки E.ccli JM103, трансформанты отбирают на селективной среде с ампициллином. Рекомбинантные ДНК со вставками нужной длины выявляют рес- триктным анализом плазмид, выделенных из полученных клонов. Нуклеотидные последовательности клонированных фрагментов подтверждают секвенированием по методу Сэнгера. Наработкой плазмид, включающих фрагменты заданных нуклео- тидных последовательностей, получают ре- комбинантныеДНКрРСО4а-19. pPCD4b-18, pPCD4c-18 соответственно, содержащие фрагмент(а)и Pst1-Kpn1 -фрагмент вектора pUC19, фрагмент (Ь) и Pst1-Kpn1 - фрагмент вектора pUC18, фрагмент (с) и Pst1-Kpn1 - фрагмент вектора pUC18.
Для получения рекомбинантных ДНК. содержащих фрагменты (ab) и (abc) и Pst1 Крп1 - фрагмент вектора pUC19, рекомби нантную ДНК pPCD4b-18 расщепляют рестриктазами Вд1П и EcoR1 и выделяют фрагмент длиной 177 п.о., смешивают его с векторной ДНК, полученной расщеплением рекомбинантной ДНК pPCD4a-19 рестриктазами Вд1П и EcoR1 и обрабатывают ДНК- лигазой. Полученной смесью трансформируют клетки E.coll JM103, трансформанты отбирают на селективной среде с ампициллином. Рекомбинантную ДНК со вставкой нужной длины выявляют рестриктным анализом плазмид, выделенных из полученных клонов. Нуклеотидную последовательность стыка подтверждают секвенированием по методу Сэнгера. Наработкой плазмиды. включающей фрагмент заданной нуклеотидной последовательности, получают рекомбинантную ДНК pPCD4ab-19. содержащую фрагмент (ah) и Pst1-Kpn1 - фрагмент вектора pUC19. Рекомбинантную ДНК pPCD4c-18 расщепля- ют рестриктазами Pst1 и EcoRI, выделяют фрагмент длиной 251 п.о., смешивают его с векторной ДНК, полученной расщеплением рекомбинантной ДНК pPCD4ab-19 ре- кстриктазами Pst1 и EcoRI и обрабатывают
0 ДНК-лигазой. Полученной смесью трансформируют клетки E.coli JM103. трансформанты отбирают на селективной среде с ампициллином. Рекомбинантную ДНК со вставкой нужной длины выявляют рестрик5 тным анализом плазмид, выделенных из полученных клонов. Нуклеотидную последовательность стыка подтверждают секвенированием по методу Сзнгера. Наработкой плазмиды. включающей фрагмент заданной
0 нуклеотидной последовательности, получают рекомбинантную ДНК pPCD4abc-19, содержащую фрагмент (abc) и Pst1-Kpn1 - фрагмент вектора pUC19.
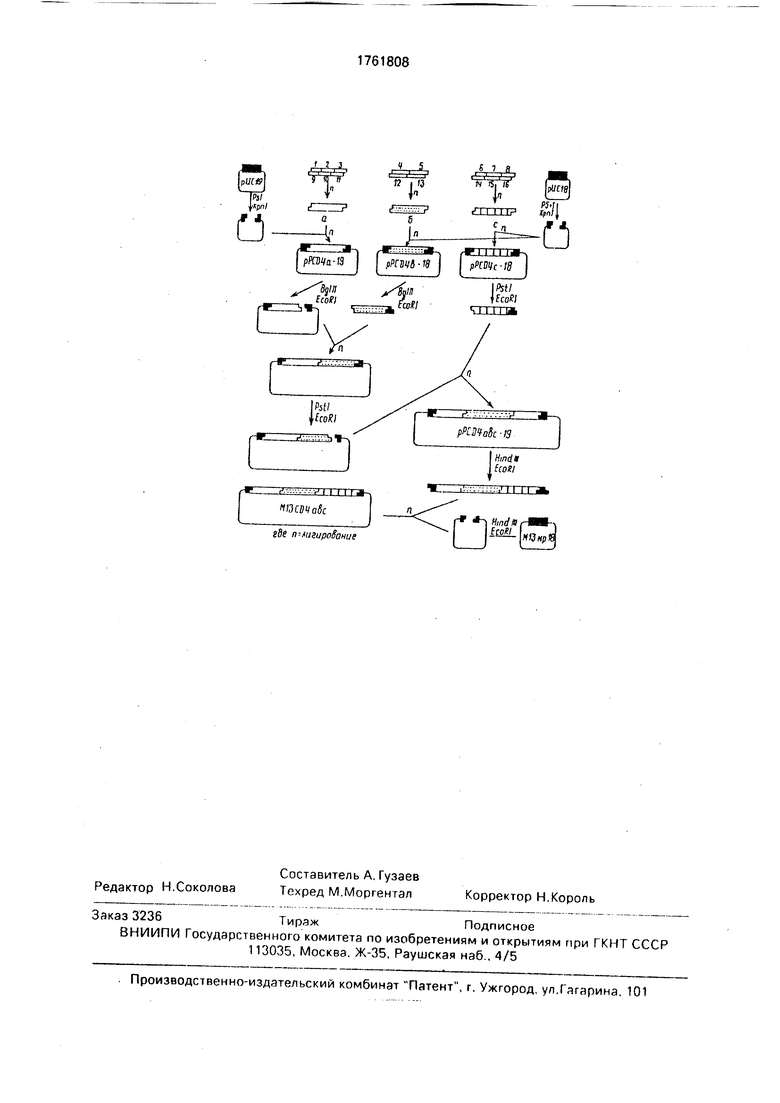
Ниже приведена схема получения всех
5 рекомбинантных ДНК.
Фрагмент (abc) переклонировали также в вектор М13тр18 Рекомбинантную ДНК pPCD4ab-19 обрабатывают рестриктазами HindLU и EcoR 1, выделяют фрагмент длиной
0 599 п.о., смешивают его с векторной ДНК. полученной расщеплением РФ-ДНК М13тр18теми же рестриктазами, и обрабатывают ДНК-лигазой фага Т4. Полученной смесью трансформируют клетки E.coll
5 JM103. Рекомбинантную ДНК со вставкой нужной длины выявляют рестриктным анализом РФ-ДНК фагов, выделенных из полученных бляшек. Наработкой ДНК, включающей фрагмент длиной 599 п.о., пол0 учают рекомбинантную ДНК M13CD4abc, содержащую фрагмент (abc) и EcoR 1-HlndUJ - фрагмент вектора М13тр18.
Сущность предлагаемого изобретения раскрывается из рассмотрения следующих
5 примеров.
П р и м е р 1. Синтез олигодезоксирибо- пуклеотида 13.
Синтез олигодезоксирибонуклеотида 13 проводят твердофазным амидофосфит0 ным методом на синтезаторе 380В (Applied Biosystems США) в шкале 0,2 мкмоль с ис- пользов- -РМ широкопористой матрицы (номина .: диаметр пор 800 А) по следующей программе: промывка и подготовка
5 мономеров 23 с, конденсация 80 с, кэпиро- вание 30 с, окисление 40 с, промывка 106 с. детритилирование 60 с, промывка 65 с В качестве мономеров используют М-ацил-5 -О-диметокситритил-3 -0-(2-цианоэтил)- М,1М-диизопропиламидофосфит -2 -дезоксирибонуклеозиды, причем если рибонуклео- зид аденозин или цитидин, то ацил бен- зоил, если рибонуклеозид гуэнозин, то ацил изобутирил, если рибонуклеозид тимидин, то ацил отсутствует В качестве активатора межнуклеотидной концентрации используют тетразол, детритилирующе- го агента 2%-ный раствор трихлоруксусной кислоты в дихлорметане, окислителя 0,1 М раствор иода в смеси пиридин-вода-тетра- гидрофуран 2:20:75, кэпирующих реагентов: равные объемы реагента А (уксусный ангид- рид-2.6-лутидин-тетрагидрофурэн 10:10:80) и реагента В (1-метилимидазол-тетрагидро- фуран 16:84), растворителя для промывки и конденсации - ацетонитрил. После завершения последнего шага наращивания цепи 5 -0-диметокситритильную группу не удаляют, готовый олигодезоксирибонуклеотид от- щепляют от матрицы 30%-ным раствором аммиака и деблокируют в том же растворе в течение 8 ч при 60°С. Летучие продукты удаляют в вакууме, остаток растворяют в 1,6 мл воды, целевой продукт выделяют методом 8ЭЖХ на колонке IMucleostl 300-5C18 (4.6x250 мм) в линейном градиенте ацето- нитрила (от 10 до 40%) в 0,05 М ацетате аммония. Собранную фракцию упаривают досуха, к остатку прибавляли 2 мл 80%-чой уксусной кислоты, выдерживают 20 мин, упаривают досуха. Остаток растворяют в 1,0 мл воды, полностью деблокированный олигодезоксирибонуклеотид выделяют методом ВЭЖХ на той же колонке в линейном градиенте ацетонигрила (от 5 до 30%) в 0.05 М ацетате аммония. Собранную фракцию упаривают досуха, дважды упаривают с 2 мл воды, растворяют в 1,0 мл воды и регистрировали УФ-спектр для определения выхода соединения 13, Воду упаривают остаток пе- реосаждают из 2%-ного перхлората лития в ацетоне. Получают 1.1 опт.ед. при Я 260 нм (о.е.), что соответствует 30 мкг олигодезок- сирибонуклеотида 13.
П р и м е р 2. Фосфорилирование олиго- нуклеотида 2 по 5 -концу. Растворяют 200 пмоль олигонуклеотида 2 в 50 мкл буфера, содержащего 50 мМ Трис-HCI (рН 7,5), 10 мМ MgCte, Ю мМ DTT, 10 мМ спермидин и АТФ в концентрации 100 пмоль/мкл, прибавляют ПНК (10 ед) и инкубируют 40 мин при 37°С. Фермент инактивируют прогреванием 65°С в течение 10 мин.
П р и м е р 3. Лигирование олигонукле- отидов 4,5,12,13. Получение фрагмента (Ь).
Фосфорилированные олигонуклеотиды 5 и 12 и нефосфорилированные 1 и 13 (по 40 пмоль каждого) смешивают в 20 мкл буфера, содержащего 50 мМ Трис-HCI (рН 7,5), 10
мМ MgCl2. прогревают при 95°С в течение 5 мин и равномерно охлаждают до комнатной температуры в течение 3 ч. Прибавляют 30 мкл буфера, содержащего 5СГмМ Трис-HCI (рН 7,5), 10 мМ MgCI2, 20 мМ DTT, 1 мМ спермидин, 1 мМ АТФ, 50 мкг/мл БСА, прибавляют ДНК-л и газу фага Т4 (2,5 ед) и инкубируют при 15°С в течение 16 ч. Продукт лигазной сшивки очищают электрофорезом в 5% ПААГ. Нужную полосу на электрофорезе выявляют при УФ освещении геля, прокрашенного бромистым этидием,
П р и м е р 4. Получение рекомбинантной ДНК, содержащей фрагмент (а) и Pst1-Kpn1- фрагмент вектора pUC 19 (pPCD4a-19).
10 пмоль фрагмента (а) смешивают в эквимолекулярном соотношении с векторной ДНК pUC 19, предварительно расщепленной рестриктазами Pst1 и Крп1, в 20 мкл буфера, содержащего 50 мМ Трис-HCI (рН 7,5), 10 мМ MgCl2, 20 мМ DTT, 1 мМ спермидин, 1 м VI АТФ, 50 мкг/мл БСА, прибавляют ДНК-лигазу фага Т4 (2,5 ед) и инкубируют при 15°С в течение 16ч. В качестве контроля используют лигирование той же векторной ДНК на себя. Опытную и контрольную пробы осаждают этанолом, растворяют каждую в 20 мкл буфера, содержащего 10 мМ NaCI, 5 мМ Трис-HCI (рН 8,0), 10 мМ MgCte и обрабатывают рестриктазой ВатЖ, сайт узнавания которой локализован только в полилинкере pUC 19 между сайтами Pst1 и Крп1. Полченной смесью трансформируют компетентные клетки E.coli JM103 и высевают на чашки с ампициллином. Получают 10- кратное превышение количества клонов в опыте над контролем. Наличие клонированного фрагмента выявляют рестриктным анализом плазмид, выделенных из полученных клонов (пример 6), а его структуру подтверждают секвенировэнием (пример 7). Плэз- миду pPCD4a-19, содержащую фрагмент (а) и Pstl-Kpnl-фрагмент вектора pUC 19. нарабатывают как описано в примере 6.
П р и м е р 5, Получение рекомбинантной ДНК, содержащей фрагмент (Ь) и Pstl-Kpnl- фрагмент вектора pUC 18 (pPCD4b-18).
10 пмоль фрагмента (Ь) смешивают в эквимолекулярном соотношении с векторной ДНК pUC 18, предварительно расщепленной рестриктазами Pst1 и Крп1, в 20 мкл буфера, содержащего 50 мМ Трис-HCI (рН 7,5), 10 мМ MS CI2, 20 мМ DTT, 1 мМ спермидин, 1 мМ АТФ, 50 мкг/мл БСА, прибавляют ДНК-лигазу фага Т4 (2,5 ед) и инкубируют при 15°С в течение 16ч. В качестве контроля используют лигирование той же векторной ДНК на себя. Опытную и контрольную пробы осаждают этанолом, растворяют каждую в 20 мкл буфера, содержащего 10 мМ NaCI,
NaCI. 5 мМ Трис-HCI (pH 8,0), 10 мМ MgCI2 и обрабатывают рестриктазой ВатШ, сайт узнавания которой локализован только в пояилинкере pUC 18 между сайтами Pst1 и Крп1. Полученной смесью трансформируют компетентные клетки E.coli JM103 и высевают на чашки с ампициллином, Получают 15- кратное превышение количества клонов в опыте над контролем. Наличие клонированного фрагмента выявляют рестриктным анализом плазмид, выделенных из полученных клонов (пример 6), а его структуру подтверждают секвенированием (пример 7), Плаз- миду pPCD4b-18, содержащую фрагмент (в) и Pstl-Kpnl-фрагментвектора pUC 18, нарабатывают как описано в примере 6.
П р и м е р 6. Выделение плазмидной ДНК.
Плазмидные ДНК выделяют методом экстракции фенол/хлороформ. Для этого 3 мл культуры E.coli, содержащей плазмиду pPCD4c-18 выращивают в течение ночи на качалке (200 об/мин) в бульоне Хоттингера, клетки осаждают центрифугированием в центрифуге Eppendorf (4 мин при 4000 об/мин). Осадок суспендируют в 200 мкл раствора, содержащего 2,5 М LiCI, 50 мМ Трис-HCI (рН 8,0), 4% (v/v Triton X-100, 62,5 мМ Na, EDTA, к полученной суспензии добавляют 200 мкл смеси фенол/хлоро- форм/изоамиловый спирт (25/24/1) и интенсивно перемешивают в течение 15 с. После центрифугирования в течение 10 мин при 14000 об/мин переносят водную фазу в новую пробирку и разбавляют в 3 раза водой. ДНК селективно осаждают центрифугированием при 14000 об/мин в течение 10 мин непосредственно после добавления в пробирку 200 мкл 40% ПЭГ 8000 и интенсивного перемешивания. Промывают осадок плазмидной ДНК 80% этанолом, высушивают в вакуумном эксикаторе и растворяют в воде. Полученную таким образом ДНК рРСО4с-18 используют для рестриктного анализа, секвенирования по методу Сэнге- ра (пример 7) и для дальнейших генноинже- нерных манипуляций (примеры 8,9).
П р и м е р 7. Секвенирование методом Сэнгера.
Денатурацию плазмидной ДНК осуществляют прибавлением 2 мкл в NaOH к раствору 4 мкг плазмидной ДНК в 20 мкл воды и инкубирование в течение 5 мин при комнатной температуре. После завершения инкубации прибавляют 6 мкл 7,5 М ацетата аммония для нейтрализации щелочи, перемешивают, прибавляют 100 мкл этанола, вновь перемешивают и замораживают в жидком азоте. Осадок ДНК собирают центрифугированием втечение 10 мин при 14000
об/мин, промывают 80% этанолом и высушивают в вакуумном эксикаторе. Растворяют осадок в 6 мкл воды, прибавляют 1 мкл буфера, содержащего 500 мМ Трис-HCI (рН
8,0), 100 мМ MgCI2 и 1 мкл праймера с концентрацией 0,2 ое/мл. Отжиг проводят 15 мин при 56°С. После завершения отжига в пробирку добавляют 2 мкл смеси, содержащей 25 мк Ки и 1,5 ед фрагмента
Кленова, аликвоты по 2,5 мкл переносят в пробирки с предварительно внесенными в них 2 мкл аликвотами терминирующих смесей и инкубируют 15 мин при 37°С. 8 пробы прибавляют по 1 мкл формамидной краски.
прогревают 10 мин при 95°С и наносят пробу на структурный гель. Радиоавтограф экспонируют на рентгеновскую пленку РМ-В.
Примерб. Получение рекомбинантной ДНК, содержащей фрагмент (а Ь) и Pst1-Kpn1
фрагмент вектора pUC 19 (pPCD4ab-19).
Рекомбинантную ДНК pPCD4b-18 расщепляют рестриктазэми Bgl11 и EcoR1 и выделяют электрофорезом в ПААГ фрагмент длиной 177 п.о. Выделенный фрагмент смешивают с векторной ДНК, полученной расщеплением pPCD4a-19, этими же рестриктазами и
очищенной электрофорезом в 1% згарозном геле, в 20 мкл буфера, содержащего 50 мМ Трис-HCI (рН 7,5). 10 мМ MgCI2. 20 мМ DTT, 1 мМ спермидин, 1 мМ АТФ, 50 мкг/мл БСА, прибавляют ДНК-лигазу фага Т4(2,5 ед) и инкубируют при 15оС в течение
16 ч. В качестве контроля лигируют векторную ДНК на себя. Полученной смесью трансформируют компетентные клетки E.coli JM 103 и высевают на чашки с ампициллином. В опыте получают 8-кратное превышение количества клонов над контролем. Наличие клонированного фрагмента выявляют рестриктным анализом плазмид, выделенных из полученных клонов (пример 6). а структуру стыка подтверждают секвенированием (пример 7).
П р и м е р9. Получение рекомбинантной ДНК, содержащей фрагмент (abc) и Hindlll- EcoR1 фрагмент вектора М13 тр18 (M13CD4abc).
Рекомбинантную ДНК pPCD4abc-19
расщепляют рестриктазами Hindlll и EcoR1 и выделяют электрофорезом в ПААГ фрагмент длиной 599 п.о. После этого данный фрагмент смешивают с векторной ДНК, полученной расщеплением РФ-ДНК фага М13 тр18 этими же рестриктазами и очищенной от короткого фрагмента линкера электрофорезом в 1 % агарозном геле, в 20 мкл буфера, содержащего 50 мМ Трис-HCI (рН 7,5), 10 мМ MgCI2, 20 мМ DTT, 1 мМ спермидин, 1
11176180812
мМ АТФ, 50 мкг/мл БСА, прибавляют ДНК-Формула изобретения лигазу фага Т4 (2,5 ед) и инкубируют при
15°С в течение 16 ч. Полученной смесьюФрагмент ДНК, кодирующий часть потрансформируют компетентные клеткиберхностного белка CD 4Т-лимфоцитов чеE.coli JM 103, которые затем высевают в5 ловека, ответственную за связывание с
полужидкий агар на индикаторные чашки,протеином др 120 вируса иммунодефицита
содержащие X-Gal и IPTG. Получают 5-крат-человека, полученный в результате твердоное превышение количества бесцветныхфазного синтеза амидофосфитным методом
бляшек над окрашенными. Наличие клони-с последующей ферментативной сборкой,
рованного фрагмента выявляют рестрикт-10 имеющий следующую нуклеотидную посленым анализом РФ-ДНК, выделенных издовательность: полученных клонов.
Таким образом, предлагаемое изобре-la+mb+nc, тение позволяет получать синтетическую
ДНК, кодирующую часть поверхностного15 где I,m,n принимают следующие значения:
белка CD4 Т-лимфоцитов человека, ответст-1 1, , , , , ,
венную за связывание с гликопротеином1 1, , . , , ,
др120 ВИЧ и ее фрагменты, отличающиеся1 0, ,
оптимизированным для E.coli кодоновымнуклеотидная последовательность а:
составом, а также рекомбинантные ДН К, со-20 держащие эти синтетические ДНК и фрагмент вектора.
TCGTTAACAAAGTTGTTCTGGGTAAAAAAGGTGACACTGTTGAACTGACTTGCACT ACGTAGCAATTGTTTCAACAAGACCCATTTTTTCCACTGTGACAACTTGACTGAACGTGA
GCTTtJTCAGAAAAAATCTATCUAGTTCCACTGGAAAAACTCTAACCAGATCAAAATCCTG
CGAAGAGTCГ ГTTTTAGATAGGTCAAGGTGACCTTTTTGAGATTGGTCTAGTTTTAGGAC
GGTAACCAGt- rTCTTTCCTGACTAAAGGTCCGTCTAAACTGAACGACCGCGCTGACTCT CCATTQGTrC AAGAAAGGACTGATTTCCAGGCAGATTTGACTTGCTGGCGCGACTGAGA
AGAAGATCTGTCGACGTAC
TCTTCTAGACAGCTG







| название | год | авторы | номер документа |
|---|---|---|---|
| ИСКУССТВЕННЫЙ ГЕН, КОДИРУЮЩИЙ ХИМЕРНЫЙ БЕЛОК АНГИОГЕНИНА ЧЕЛОВЕКА, ХИМЕРНАЯ ПЛАЗМИДА pJZZ-A, ОБЕСПЕЧИВАЮЩАЯ ЭКСПРЕССИЮ ГЕНА ХИМЕРНОГО БЕЛКА АНГИОГЕНИНА ЧЕЛОВЕКА В Escherichia coli И ШТАММ Escherichia coli BL21(DE3)/pJZZ-A-ПРОДУЦЕНТ РЕКОМБИНАНТНОГО ХИМЕРНОГО БЕЛКА АНГИОГЕНИНА ЧЕЛОВЕКА | 2012 |
|
RU2512527C2 |
| Рекомбинантная плазмидная ДНК @ -1 @ 1-13, кодирующая синтез фибробластного интерферона ( @ I) человека, способ ее конструирования, штамм бактерий ЕSснеRIснIа coLI - продуцент @ I-интерферона человека | 1987 |
|
SU1703692A1 |
| Рекомбинантная плазмидная ДНК @ - @ 2-19, кодирующая синтез интерлейкина-2 человека, способ ее конструирования @ штамм бактерий ЕSснеRIснIа coLI - продуцент интерлейкина-2 человека | 1987 |
|
SU1703693A1 |
| Способ конструирования гена интерлейкина-2 человека | 1988 |
|
SU1554382A1 |
| Рекомбинантная плазмидная ДНК РЕК 8, кодирующая фибринолизин YeRSINIa реSтIS, способ ее конструирования и штамм бактерий ЕSснеRIснIа coLI - продуцент фибринолизина YeRSINIa реSтIS | 1990 |
|
SU1751206A1 |
| Рекомбинантная плазмидная ДНК @ 10FMD, кодирующая гибридный белок Р204-AS @ Р @ С @ С @ - VPI/200-213/ Р @ Р @ S @ Р @ ( 131-160) и штамм бактерий ЕSснеRIснIа coLI -продуцент гибридного белка Р204- А @ Р @ С @ С @ V PI/200-213/-Р @ Р @ S @ Р @ - VPI /131-160/ | 1990 |
|
SU1724691A1 |
| РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК pTrcTREN-IL-13, КОДИРУЮЩАЯ ПОЛИПЕПТИД СО СВОЙСТВАМИ ИНТЕРЛЕЙКИНА-13 ЧЕЛОВЕКА, И ШТАММ БАКТЕРИЙ Escherichia coli BL21(ДЕЗ)/pTrcTREN-IL13-ПРОДУЦЕНТ ПОЛИПЕПТИДА СО СВОЙСТВАМИ ИНТЕРЛЕЙКИНА-13 ЧЕЛОВЕКА | 2006 |
|
RU2333960C1 |
| РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК PLT 9, КОДИРУЮЩАЯ ПОЛИПЕПТИД СО СВОЙСТВАМИ ЛИМФОТОКСИНА ЧЕЛОВЕКА, РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК PLT 16, ИСПОЛЬЗУЕМАЯ ДЛЯ КОНСТРУИРОВАНИЯ ДНК PLT 9, И ШТАММ БАКТЕРИЙ ESCHERICHIA COLI - ПРОДУЦЕНТ ПОЛИПЕПТИДА СО СВОЙСТВАМИ ЛИМФОТОКСИНА ЧЕЛОВЕКА | 1988 |
|
SU1561510A1 |
| Рекомбинантная плазмидная ДНК @ HRAST @ =3, кодирующая онкоген HRAS=1 карциномы щитовидной железы человека, и способ ее конструирования | 1990 |
|
SU1815273A1 |
| Рекомбинантная плазмидная ДНК @ 14, кодирующая полипептид, со свойствами лейкоцитарного интерферона @ 2 человека, и штамм бактерий ЕSснеRIснIа coLI - продуцент полипептида со свойствами лейкоцитарного интерферона @ 2 человека | 1990 |
|
SU1703691A1 |
Использование: молекулярная биология, генноинженерная биотехнология. Сущность изобретения: получена синтетическая ДНК abc с оптимизированным для Е scherichia coli кодоновым составом, кодирующая область ABC: 1-185 поверхностного белка СД4 Т-лимфоцитов человека, ответственная за связывание с гликопротеином др 120 вируса иммунодефицита и ее фрагментов a,b,c, ab, кодирующих соответственно области СД4, А: 1-60, В: 59-110, С: 109-185, АВ: 1-110. Фрагмент а с кодируют два концевых домена СД4 субфрэгмента а - первый центр связывания с гликопротеином др 120 ВИЧ, субфрагмент b - второй центр связывания, субфрагмент с - второй домен белка СД4, субфрагмент ab - оба центра связывания. 1 ил. (Л С xi о 00 О 00 
нуклеотидная последовательность b :
GATCTCTGTGGGACCAGGGTAACTTCCCGCTGATCATCAAAAACCTG ACGTCTAGAGACACCCTGGTCCCATTGAAGGGCGACTAGTAGTTTTTGGAC
AAAATC3AAGACTCTGACACTTACATCTGCGAAGTTGAAGACCAGAAAGAAGAAGTTCAG TTTTAGCTTCTGAGACTGTGAATGTAGACGCTTCAACTTCTGGTCTTTCTTCTTCAAGTC
CTGCTGGTTTTCGGTCTGACTGCTAACTGTGACACTCACCTGCTGCAGGTCGACGTAC GACGACCAAAAGCCAGACTGACGATTGAGACTGTGAGTGGACGACGTCCAGCTG .
AC
13176180814
иуклеотидная последовательность с :
TraTGC:AGG(JTCAGTCTCTGACTCTGACTCTGGAATC TCCCCCGGGTTCTTCTCCG CGTAGGACGTCCCAGTCAGAGACTGAGACTGAGACCTTAGAGGGGGCCCAAGAAGAGGC
TCTGTTCAGTGCCC€TCTCCGCGCGGTAAAAACATCCAGGGTGGTAAAACTCTGTCTGTT AGAOAAGTCACGGCGAGAGGCGCGCCATTTTTGIAGGTCCCACCATTTTGAGACAGACAA
TCTCAGCTGGAACTGCAAGACTCTGGTACT-IGGACTTGCACTGTTCTGCAAAACCAGAAA AGAGTCGACCTTGACGTTCTGAGACCATGAACCTGAACGTGACAAGACGTTTTGGTCTTT
AAAGTTGAGTTCAAAATCGATATCGTTGTTCTGGCTTTCCAGAAAGCCTCATCGATTGTC TTTCAACTCAAGTTTTAGCTCTAGCAACAAGACCGAAAGGTCTTTCGGAGTAGCTAACAG
GACGTAC
CTG, , ,
...O- M
AOAAAGTTGTTCTC:. V.T. A U. A T/n - AC ACTGT l 0 A ftCTGACTTCCACTGCTTCTCAGA АССТАГ,( ААТТОТТТСААСААСЛСССА1Т-ГТТи А г-ТГТ -/уСМ :ТТСАСТСЛЛСГ;ТПАССЛАСЛСТСТ
|... --ПЛ..- -. - 0 ( Г V --I------- J----J- --- J I- - -TJ- ---
AAAAATCrATCCAGTTCCACTGGAAAAACTrTAACCAGATCAAAATCCTGGGTAACCAGGGTTCTTTCCT TnTTAfiATAGGTCAAIGTGACCT-T TT i GAGrtTTGGTCTA JT ГТ rAC ACCCATTGGTCCCAAGAAAGGA - - i- n( y)
w.l
-ilol i ,
GACTAAAGGTCCGTCTAAACTGAACGACCGCGCTGACTCTAGAAGATCTGTCGACGTAC фрагмент
СТСАТТТСГАГ.Г,ГА ;АТТТГ;ЛПТТСС г-г.с СГСАГП: v ATCTTtrrAGACAGcr а
IJI ft 1:
j4 ( ah )
nATCTCTGTGGGACCAGGG IAAi TCCCnClGATCATCAAAAACCTGAAAATCGAAGACTCTGACA ACGTCTAGAGACACCCTGGT CCATTGAAGG.3CGACTAGTAGTTTTTGGACTTTrAGCTTCTGAGACTGT
r„ilTeol
, I,.
CTTACATCTGGGAAGTTGAACACCAGA ACAАПА ArjTTCACCTGCTCGTlTTCGGTCTGACTGCTAACTC
GAATGTAGACGCTTCAAC TTCTGGTClTTC1TCTICAAGTCGACGACCAAAAGCCAGACTGACGATTGAG
ц:
5 в01|
TGACACTCACCTGCTGCAa:TCGACGl Cфрагмрнт в
ACTG rGAGTGGACGACGTCiJACC I (,
3(05 I
-1
rCCTGCAGGGTCAGTCTC 1 GACl О ТСы 1ГЛ GCAATC1 COuCCGG ГГТСТТС 1 CCG ГСТСТТСЛГ.
лсстАсплсстсссАс;тсАг.Аг;Астслглстг.А :дс:г:ттАС.лппа:СтСС (:/ AGA AGAGGCAGACAAGTCA PнТтм
GCCGCTCTCCGCGCGGTAAAAACATC( GG1A AA ACTC i GT CTGTTTCTCAGCTGGAACTGCAAGA CGGCGAGAGGCGCGCCATTTTTGTAGGTf:CCACrATTTlf.AGAr:AGACAAAGAGTCGACCTTGACGTTCT
I I --. . . -7(82)
-ЧCTCTGGTAC TTGGACTTGCAClGTTCi a:/ AAArCV,(;A AAAAGTTGAGTTCAAAATCGATATCGTTGTT
GAGACCATGAACCTGAACfJTGACAAGACCTI TCCTC ГГТ ГТТСААСТСАAGTTTTAGCTCTAGCAACAA
T - i .
15(62)
6(80),
CTGGCTTTCCAGAAAGCCTCATCGATTGICGA ,&TAC
GACCCAAAGGTCTTTCGGAGTAGCTAACAr;.T |
TO-TTAACAAAGTTGTTCTGCKTAAAAAAG&TUACACTGTTGAACTGACTTGCACTGCTTCU .. ACGTAGCлATTGTTTCAACAAGACCCATTTTTTCCACTGTGACAACTTGACTGAACGTGACGAAGAulCT
AAAAATCTATCCAGTTCCACTGGAAAAACTCTAACCACATCAAAATCCTGGGTAACCAGGGTTCTnC(-l TTTTTAGATAGGTCAAGGTGACCTTTTTGAGATTGGTCTAGTTTTAGGACCCATTGGTCCCAAGAAAGoA
CACTAAAGGTCCGTCTAAACTGAACGACCGCGCTGACTCTAGAAGATCTCTGTGGGACCAGGGTAACTTC CTGATTTCCAGGCAGATTTGACTTGCIGGCGCGACTGAGATCTTCTAGAGACACCCTGGTCCCATTGAAG
CCGCTGATCATCAAAAACCTGA AATCGAAGACTCTGACACTTACATCTGCGAAGTTGAAGACCAGAAAG GGCGACTAGTAGTTTTTGGACTTTTAGC1TCTGAGACTGTGAATGTAGACGCTTCAACTTCTGGTCTTTC
AAGAAGTTCAGCTGCTGGTTTTCGGTCTGACTGCTAACTCTGACACTCACCTGCTGCAGGTCGACGTAC TTCTTCAAGTCGACGACCAAAAGCCAGACTGACGATTGAGACTGTGAGTGGACGACGTCCAGCTG
17618081Г
(j 00 I
TCGTT AACAAAGTTGTTCTGGGTAAAAAAGGTGACACTGTTGAACTGACTTGCACT ACGTAGCAA TTGTTTCAACAAGACCCATTTTTTCCACTGTGACAACTTGACTGAACGTGA
GCTTCTCAGAAAAAATCTATCCAGTTCCACTGCAAAAACTCTAACCAGATCAAAATCCTG CCAAGAGTCTTTTTTAGATAGGTCAAGCTGACCTTTTTGAGATTCGTCTAGTTTTACCAC
GGTAACCAGGGTTCTTTCCTGACTAAAGGTCCGTCTAAACTGAACGACCGCGCTGACTCT CCATTGGTCCCAAGAAAGGACTGATTTCCAGGCAGATTTGACTTGCTGGCGCGACTGAGA
AGAAGATCTCTGTGGGACCAGGGTAACTTCCCGCTGATCATCAAAAACCTGAAAATCGAA TCTTCTAGAGACACCCTGGTCCCATTCAAGGGCGACTAGTAGTTTTTGGACTTTTAGCTT
GACTCTGACACTTACATCTGCGAAGTTGAAGACCAGAAAGAAGAAGTTCAGCTGCTGGTT CTGAGACTGTGAATGTAGACGCTTCAACTTCTGGTCTTTCTTCTTCAAGTCGACGACCAA
TTCGGTCTGACTGCTAACTCTGACACTCACCTGCTGCAG GTCGACGTAC AAGCCAGACTGACGATTGAGACTGTGAGTGGACGACGTC CAGCTG
где n-HizupoSoHue
Авторы
Даты
1992-09-15—Публикация
1990-08-10—Подача